1. 재조합 단백질 용해성 문제 해결의 근본적 접근
바이오 의약품 및 연구용 단백질 생산 시 가장 빈번하게 마주치는 문제는 단백질이 정상적으로 접히지 않고 거대한 응집체인 봉입체(Inclusion Bodies)를 형성하는 것입니다. 특히 대장균(E. coli)과 같은 원핵생물 숙주에서 진핵생물 유래 단백질을 과발현할 때 이러한 현상이 두드러집니다 (ScienceON, 2022).
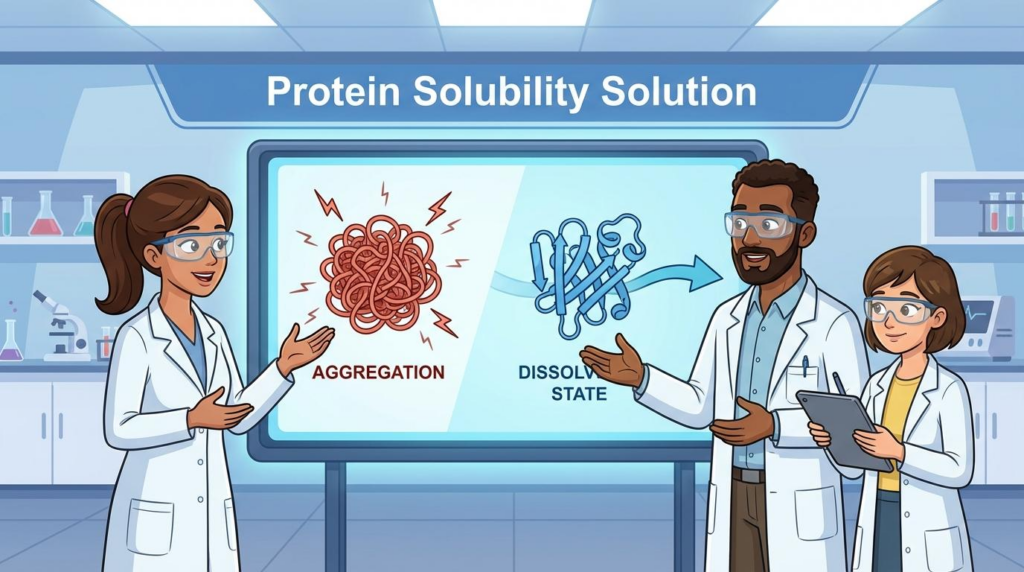
단백질은 왜 뭉치는가? (Aggregation Mechanisms)
- 과도한 발현 속도: 숙주 세포 내 단백질 생산 속도가 Chaperone의 접힘(Folding) 처리 능력을 초과할 때 발생합니다.
- 소수성 노출: 단백질 내부로 숨어야 할 소수성 아미노산 잔기들이 외부로 노출되면서 분자 간 비특이적 결합이 일어납니다.
- 환경 불일치: 숙주 세포의 pH, 이온 강도, Redox 환경이 목적 단백질의 안정적 구조 형성에 부적합한 경우입니다.
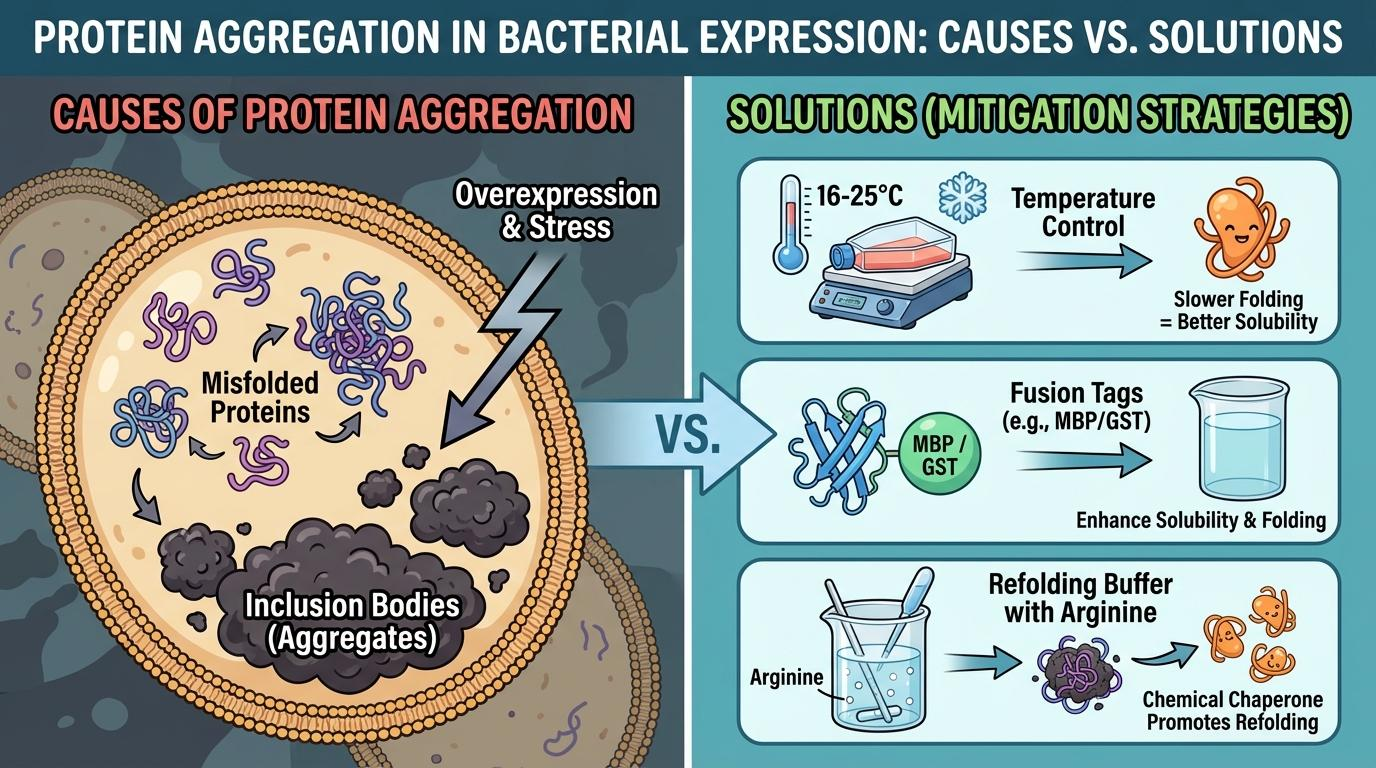
[그림 1] 단백질 응집 발생 원인 및 주요 공정 개선 단계
2. 단백질 Solubility 개선을 위한 발현 최적화
가장 효율적인 불용성 단백질 해결 방법은 이미 뭉친 것을 푸는 것이 아니라, 처음부터 뭉치지 않게 발현 조건을 조절하는 것입니다.
저온 배양 전략 (16-25°C)
배양 온도를 낮추면 단백질 합성 속도가 지연되어 숙주 세포의 Chaperone이 접힘을 도울 수 있는 충분한 시간을 확보하게 됩니다. 실제 연구 데이터에 따르면, 37°C에서 5%에 불과했던 가용성 단백질 비율이 18°C 배양 시 65%까지 증가한 사례가 보고되었습니다.
Fusion Tag의 활용
특정 용해성 증진 태그를 단백질 N-말단에 결합하면 전체 복합체의 Solubility가 크게 향상됩니다.
| 전략 유형 | 주요 장점 | 성공률(예시) |
|---|---|---|
| MBP (Maltose Binding Protein) | 가장 강력한 용해성 증진 효과 | 약 70% 이상 |
| GST (Glutathione S-transferase) | 정제 편의성 및 용해도 향상 | 약 50% 내외 |
| Arginine 첨가 (Refolding) | 비특이적 응집 억제 | 수율 20-50% 향상 |
3. 봉입체 단백질 처리 및 Refolding 기술
발현 최적화에도 불구하고 뭉침 현상이 발생한다면, 봉입체를 수거하여 다시 접는(Refolding) 과정을 거쳐야 합니다.
강력한 변성제 사용
6-8M Urea 또는 6M Guanidine-HCl을 사용하여 단백질을 완전히 풀어준 뒤, 투석(Dialysis)이나 희석(Dilution)법을 통해 서서히 변성제를 제거합니다. 이때 GSH/GSSG와 같은 Redox Pair를 적절히 배합하여 올바른 Disulfide Bond 형성을 유도하는 것이 핵심입니다.
Refolding 버퍼에 0.4~1.0M Arginine을 첨가해 보세요. Arginine은 단백질 분자 간의 비특이적 상호작용을 차단하여 응집을 막아주며, 최종 수율을 최소 2배 이상 높여주는 ‘Magic Reagent’ 역할을 합니다.
4. HEK/CHO 세포에서의 Aggregation 문제
포유류 세포 시스템은 PTM(번역 후 변형) 능력 덕분에 대장균보다 용해성이 우수하지만, 여전히 뭉침 현상이 발생합니다.
- HEK293: Transient 발현 시 ER 스트레스 및 고밀도 배양에 따른 Apoptosis로 단백질 품질 저하.
- CHO: Sialic Acid 결합 방식(alpha 2-3) 차이 및 비인간형 Glycan 구조로 인한 소수성 노출 및 응집 촉진.
5. 자주 묻는 질문 (FAQ)
Q1. 퓨전 태그를 사용하면 단백질 기능에 영향이 없나요?
A1. 태그가 기능을 방해할 수 있으므로, 태그와 목적 단백질 사이에 Protease 인식 부위(TEV, Thrombin 등)를 넣어 정제 후 태그를 제거하는 공정이 권장됩니다.
Q2. Refolding 과정에서 수율이 너무 낮습니다.
A2. 단백질 농도를 0.1mg/mL 이하로 매우 낮게 유지하며 천천히 변성제를 제거하십시오. 농도가 높을수록 다시 뭉칠 확률이 기하급수적으로 높아집니다.
핵심 용어 정리 (Glossary)
- Inclusion Bodies (봉입체)
- 불완전하게 접힌 단백질들이 세포 내에서 서로 뭉쳐 형성된 불용성 응집체.
- Chaperone (샤페론)
- 세포 내에서 다른 단백질이 올바른 3차원 구조로 접히도록 도와주는 도우미 단백질.
- Codon Optimization (코돈 최적화)
- 숙주 세포에서 잘 쓰이지 않는 희귀 코돈을 선호 코돈으로 교체하여 번역 효율과 접힘 품질을 높이는 기술.
* 본 포스팅에 언급된 상표 및 제품명은 해당 소유권자의 자산이며, 정보 제공 목적으로만 사용되었습니다.
문의 QR 코드 (메시지 연결)