항체 의약품의 임상 성공을 위해서는 단순 친화도(Affinity)보다 실제 효능을 반영하는 avidity 평가가 중요합니다. 살아있는 세포 표면을 모사하는 LigandTracer와 고해상도 SPR 분석을 병행함으로써, 항체의 이가 결합(Bivalency)과 재결합(Rebinding) 효과가 약효 지속 시간(Target occupancy)에 미치는 영향을 정밀하게 분석할 수 있습니다.
대학원 연구실에서 밤늦게까지 FACS 데이터를 정리하며 한 가지 의문에 빠진 적이 있으신가요? “단백질 수준의 SPR 분석에서 얻은 KD 값은 우수했는데, 왜 실제 세포 실험(In-vitro) 결과는 그에 못 미칠까?” 이는 바이오 벤처의 연구원이나 팀장급 연구자들이 프로젝트 진행 중 가장 흔히 맞닥뜨리는 ‘Affinity의 함정’입니다.
세포 표면의 항원은 고정되어 있지 않고 유동적이며, 항체는 두 개의 팔(Bivalent)을 통해 다가성 결합을 형성합니다. 따라서 단순히 1:1 모델로 결합력을 측정하는 것만으로는 충분하지 않습니다. 이제는 avidity 평가를 통해 항체가 타겟에 얼마나 안정적으로 머무르는지를 과학적으로 증명해야 합니다.
1. 왜 avidity 평가가 항체 개발의 핵심인가?
항체의 avidity 평가는 단일 결합 세기인 Affinity와 항체의 구조적 지오메트리(Geometry), 그리고 항원의 밀도가 결합하여 나타나는 ‘총체적 결합 세기’를 분석하는 과정입니다.
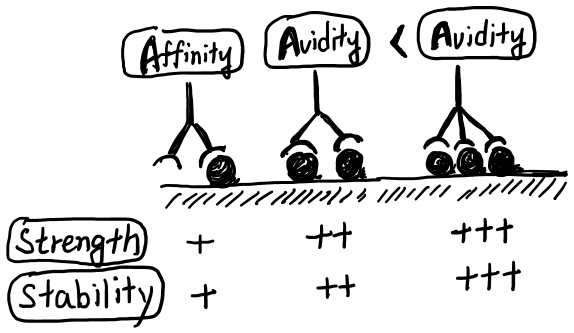
실제 연구 현장에서 avidity 평가가 중요한 이유는 다음과 같습니다:
- 재결합 효과(Rebinding Effect): 한쪽 팔이 떨어져도 다른 쪽 팔이 붙어있어 전체 결합을 유지하는 능력을 평가합니다.
- 타겟 점유율(Target Occupancy) 예측: 약물이 체내에서 타겟에 얼마나 오랫동안 머무를지 예측하여 투여 주기를 최적화합니다.
- 생체 모사도 향상: 정제 단백질 환경이 아닌 실제 세포 표면 환경에서의 결합력을 대변합니다 (Heirene et al., 2024).
해리 속도(kd)가 매우 느린 항체를 선별하고 있다면, 단순 KD 값보다 Residence Time을 확인하십시오. Avidity가 높은 항체는 낮은 농도에서도 높은 점유율을 유지하여 효능(Efficacy)을 비약적으로 높일 수 있습니다.
2. 분석 기술별 avidity 평가 특징 비교
SPR, BLI, LigandTracer 등 다양한 기술을 통해 avidity를 평가할 수 있지만, 각각의 분석 환경과 제공하는 인사이트에는 차이가 있습니다.
| 특징 | SPR 분석 | BLI 분석 | LigandTracer |
|---|---|---|---|
| 분석 환경 | 정제 단백질 (센서 칩) | 정제 단백질 (센서 팁) | 살아있는 세포 (Live Cells) |
| avidity 평가 방식 | Bivalent 모델 피팅 | 랭킹 및 단순 비교 | 세포 표면 직접 측정 |
| 생체 모사도 | 중간 (고정 밀도 조절 필요) | 낮음 | 매우 높음 (37°C 환경 가능) |
3. LigandTracer: 실시간 세포 기반 avidity 평가의 표준
정제 단백질을 사용하는 고전적 방식의 한계를 극복하기 위해 LigandTracer를 활용한 avidity 평가가 각광받고 있습니다. 이는 살아있는 세포를 배양한 상태에서 항체의 결합 역학을 실시간으로 추적합니다.
세포 기반 분석이 제공하는 핵심 인사이트
- 세포 내재화(Internalization) 구분: 결합 후 세포 안으로 들어가는 속도를 파악하여 ADC 의약품 개발에 필수적인 데이터를 제공합니다.
- Interaction Map: 결합의 균질성을 시각화하여 1가 결합과 2가 결합이 섞여 있는 양상을 분석합니다 (Bondza et al., 2020).
- 장시간 해리 측정: Avidity 효과로 인해 매우 느리게 떨어지는 항체의 kd 값을 안정적으로 산출합니다.
4. 적용 효과: avidity 평가로 입증하는 파이프라인 가치
체계적인 avidity 평가 데이터를 확보한 후보 물질은 단순 Affinity 데이터만 있는 물질보다 높은 시장 가치를 가집니다.
- 임상 진입 가속화: 동물 실험 전 효능 예측력을 높여 시행착오를 줄입니다.
- 독성 및 부작용 감소: 타겟 선택성이 높은 ‘Avidity-rich’ 후보 물질을 선별할 수 있습니다.
- 기술 수출(License-out) 강화: 글로벌 제약사가 요구하는 고수준의 kinetics 근거 자료를 제시할 수 있습니다.
? 자주 묻는 질문 (FAQ)
A: 항체의 두 팔이 항원과 동시에 결합할 때 발생하는 시너지 효과(Synergy effect) 때문입니다. 재결합 확률이 비약적으로 높아지면서 겉보기 해리 속도(apparent kd)가 훨씬 느려지게 됩니다.
A: 네, 매우 중요합니다. 세포 표면의 항원 밀도와 수용체 클러스터링 상태에 따라 결과가 달라지므로, 타겟 질환과 유사한 세포주를 선택하는 것이 분석의 핵심입니다.
정밀한 avidity 평가로 연구의 수준을 높이십시오
불확실한 데이터로 고민하지 마세요. 와이클루바이오가 생물학적으로 가장 유의미한 실시간 kinetics 수치를 제공해 드립니다.
전문 상담 및 서비스 문의하기참고문헌
- • Bondza, S., ten Broeke, T., Nestor, M., Leusen, J. H. W., & Buijs, J. (2020). Bivalent binding on cells varies between anti-CD20 antibodies and is dose-dependent. mAbs, 12(1), 1792673.
- • Heirene, L. A., Byrne, H. M., Gaffney, E. A., & Yates, J. W. (2024). Understanding Antibody-Target Antigen Interactions and the Avidity Effect Using Mathematical Modelling. bioRxiv.
- • Pratesi, F., et al. (2021). BNT162b2 mRNA SARS-CoV-2 Vaccine Elicits High Avidity and Neutralizing Antibodies in Healthcare Workers. Vaccines, 9(6), 672.

