Binding Affinity Analysis 시 SPR과 BLI 결과가 다른 핵심 이유는 유체 흐름(Flow) 유무에 따른 질량 전달 제한(MTL)과 재결합(Rebinding) 현상 때문입니다. SPR은 정밀한 속도 상수를 제공하는 반면, BLI는 Crude 샘플 분석에 강점이 있으나 해석 시 Diffusion 효과와 Baseline Drift를 반드시 보정해야 정확한 결합 친화도 산출이 가능합니다.
“동일한 샘플인데, 왜 KD 값이 3배 이상 차이 날까요?”
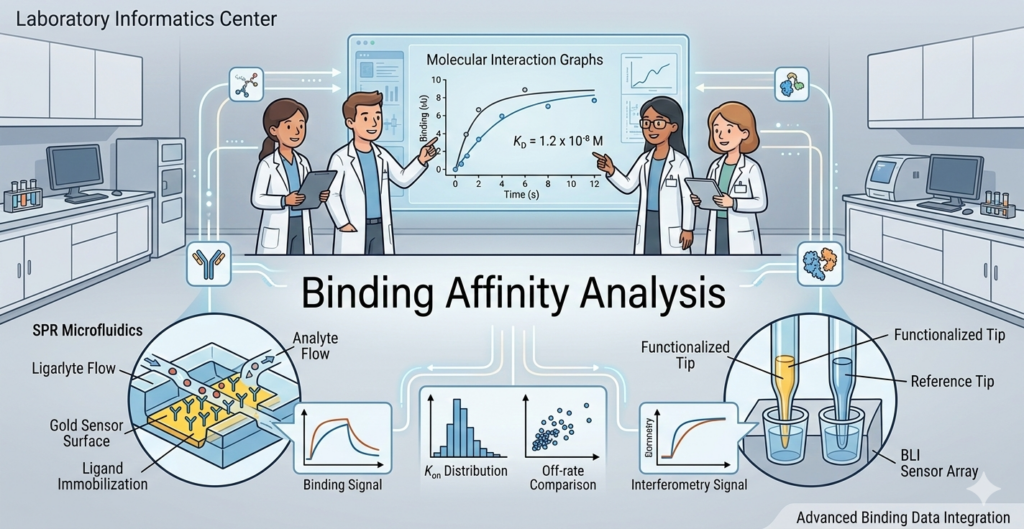
바이오 벤처나 대학원 연구실에서 항체 혹은 단백질의 결합 친화도(Binding Affinity)를 측정할 때 가장 당혹스러운 순간은 SPR(Surface Plasmon Resonance)과 BLI(Bio-Layer Interferometry) 데이터가 일치하지 않을 때입니다. 분명 같은 항원과 항체임에도 불구하고, 한쪽에서는 nM 단위가 나오고 다른 쪽에서는 수십 nM이 나오는 경우가 허다합니다.
많은 연구자가 이를 ‘장비의 오차’로 치부하곤 하지만, 사실 이는 분석물이 센서 표면에 도달하고 해리되는 물리적 환경의 차이에서 기인합니다. 특히 Binding Affinity Analysis의 핵심인 kon(결합 속도)과 koff(해리 속도) 값이 시스템별로 어떻게 다르게 피팅되는지 이해하는 것이 중요합니다.
Binding Affinity Analysis: SPR vs BLI 시스템 비교
두 기술은 모두 라벨 없이(Label-free) 실시간 상호작용을 측정하지만, 시료를 다루는 방식에서 극명한 차이를 보입니다.
1. 연속 흐름(Continuous Flow) vs 웰 내 교반(Orbital Shaking)
SPR은 마이크로 유체 채널을 통해 신선한 버퍼를 지속적으로 공급하는 연속 흐름 시스템입니다. 이는 해리 단계에서 센서 표면에서 떨어진 분석물을 즉시 채널 밖으로 씻어내어 재결합(Rebinding)을 물리적으로 차단합니다.
반면, BLI는 센서를 샘플 웰(Well)에 담그는 ‘Dip-and-read’ 방식입니다. 물론 BLI 장비도 플레이트를 흔들어 주는 Orbital Shaking(교반)을 수행하지만, 이는 웰이라는 ‘닫힌 시스템’ 내에서의 순환입니다. 즉, 해리된 분자가 샘플 용액 밖으로 완전히 제거되지 않고 센서 주변에 머물 가능성이 SPR보다 훨씬 높으며, 이로 인해 koff 값이 실제보다 느리게 측정되는 경향이 여전히 존재합니다.
심층 분석: 확산층(Diffusion Layer)과 교반의 역할
센서 표면 바로 위에는 유체의 흐름이 거의 멈춰있는 정적 경계층(Stagnant Boundary Layer)이 형성되는데, 이를 확산층(Diffusion Layer)이라고 부릅니다. 용액 속의 분석물(Analyte)이 리간드와 결합하려면 반드시 이 층을 통과해야 합니다.
- 왜 얇게 만들어야 하나? 확산층이 두꺼우면 분석물이 표면에 도달하는 속도가 느려집니다. 이 경우 측정되는 kon 값은 실제 결합 속도가 아니라 ‘분자가 확산되는 속도’에 의해 결정되는 질량 전달 제한(Mass Transport Limitation) 현상이 발생합니다.
- 얇아지는 원리: SPR에서의 높은 유속(Flow rate)이나 BLI에서의 강한 교반(Shaking RPM)은 물리적인 힘으로 정적 경계층을 밀어냅니다. 유체 역학적으로 대류(Convection)가 강해질수록 확산에만 의존해야 하는 거리가 짧아지므로 실제 결합력을 더 정확하게 포착할 수 있습니다.
2. 감도의 역설: 왜 BLI는 지저분한 샘플에 강한가?
일반적으로 “감도가 낮다”는 것은 단점으로 여겨지지만, Binding Affinity Analysis에서 BLI의 낮은 감도는 오히려 Crude 샘플(배양액, 혈청 등) 분석 시 강력한 무기가 됩니다.
SPR은 용액의 굴절률 변화에 극도로 예민합니다. 배양액처럼 단백질과 불순물이 뒤섞인 용액을 흘리면, 분석물의 결합 신호보다 용액 자체의 배경 굴절률(Bulk Effect) 변화가 훨씬 크게 나타나 실제 신호를 가려버립니다. 반면, BLI는 빛의 간섭 현상을 이용하여 센서 끝단의 ‘생물학적 층(Biolayer)’의 두께 변화만 측정합니다.
kon koff 값 피팅 모델의 차이점
데이터 해석 시 연구원들이 가장 많이 실수하는 부분은 피팅 모델(Fitting Model)의 선택과 Baseline 관리입니다.
잠깐! Baseline Drift가 무엇인가요?
Baseline Drift란 상호작용이 없는 상태에서도 시글널이 평평하지 않고 시간이 지남에 따라 점진적으로 상승하거나 하락하는 현상을 말합니다. 주로 다음과 같은 상황에서 발생합니다.
- 리간드 탈리(Leaching): 센서에 고정된 리간드가 결합이 약해 해리 단계에서 조금씩 떨어져 나가는 경우 (하향 드리프트).
- 버퍼 불일치: 샘플 버퍼와 러닝 버퍼의 조성(pH, Salt 등)이 미세하게 달라 굴절률이 변하는 경우.
- 온도 변화: 장비 내부 온도가 미세하게 출렁이며 센서의 물리적 특성이 변하는 경우.
Local Fitting이 KD 값을 왜곡시키는 이유
SPR에서 주로 쓰는 Global Fitting은 여러 농도의 곡선을 동시에 최적화합니다. kon과 koff는 상수로 고정되므로, 특정 농도 곡선에 미세한 드리프트가 있어도 전체 데이터의 평균적인 흐름으로 이를 상쇄할 수 있습니다.
하지만 BLI에서 자주 사용되는 Local Fitting은 각 농도별 곡선을 독립적으로 피팅합니다. 만약 100 nM 농도의 곡선에서 리간드 탈리로 인해 하향 드리프트가 발생했다면, 소프트웨어는 이를 ‘분석물이 매우 빠르게 떨어져 나가는 것’으로 오해하여 koff 값을 실제보다 훨씬 크게 계산하게 됩니다. 결과적으로 해당 농도의 KD 값은 실제보다 훨씬 높게(낮은 친화도) 왜곡되어 나타납니다.
보고받은 데이터에서 BLI의 KD 값이 SPR보다 비정상적으로 좋게(낮게) 나왔다면, Avidity effect(결합가 효과)를 의심해보십시오. 리간드 고정 농도가 너무 높으면 다중 결합이 발생하여 koff 값이 실제보다 훨씬 느리게 계산될 수 있습니다. 이럴 땐 리간드 밀도를 절반 이하로 낮춘 재실험이 필요합니다.
실제 데이터 해석 사례
동일한 항체 시료를 분석했을 때 나타날 수 있는 전형적인 차이의 예시입니다. 단위 표기 시 지수 부분을 주의 깊게 확인하십시오.
- SPR 측정 결과:
kon = 1.0 × 105 M-1s-1
koff = 1.0 × 10-4 s-1
→ KD = 1.0 nM - BLI 측정 결과:
kon = 2.5 × 105 M-1s-1 (Diffusion 영향으로 과대 추정 가능성)
koff = 5.0 × 10-4 s-1 (Baseline Drift 반영 가능성)
→ KD = 2.0 nM
자주 묻는 질문 (FAQ)
Q1: 비특이적 결합이 너무 심해 피팅이 안 됩니다. 어떻게 하나요?
A: 버퍼에 BSA(0.1-1%) 혹은 Tween-20을 추가하고, SPR의 경우 카르복시메틸 덱스트란 함량이 적은 칩으로 교체하는 것이 효과적입니다.
Q2: 논문 투고 시 어떤 데이터를 더 신뢰하나요?
A: 학계에서는 전통적으로 SPR 데이터를 ‘Gold standard’로 간주합니다. 하지만 BLI 데이터도 충분한 대조군(Negative control)과 Orthogonal validation 데이터가 동반된다면 충분히 신뢰받을 수 있습니다.
참고문헌
- • Sartorius. BLI vs SPR: Choosing the ideal method for analyzing biomolecular interactions. Sartorius Blog.
- • GenScript. BLI & SPR Real-time affinity measurement services. GenScript Technical Guide.
- • YClueBio. SPR vs BLI Molecular Binding Analysis Comparison. YClueBio Insights.
- • Nicoya Life. Comparison Study: Label-free Biosensors Performance. Nicoya White Paper.
- • Malvern Panalytical. BLI vs SPR vs GCI: Grating-Coupled Interferometry. Technical Review.
문의 QR 코드 (메시지 연결)