1960년대 초기 효소 기반 혈당 측정기에서 시작된 바이오센서는 지난 반세기 동안 비약적인 발전을 거듭해 왔습니다. 특히 현대 바이오 의학 연구의 핵심인 항체-항원 결합 분석은 정적인 결과만을 제공하던 ELISA 시스템에서, 분자 간의 ‘밀당’을 실시간으로 포착하는 SPR(Surface Plasmon Resonance) 기술로 그 중심축이 이동하고 있습니다.
바이오센서는 왜 SPR로 진화했는가? 전통적인 ELISA는 표지(Label)가 필요하고 다단계 세척 과정에서 저친화력 결합 정보를 소실하기 쉽습니다. 반면 최신 SPR 기술은 레이블프리(Label-free) 방식으로 분자 결합(ka)과 해리(kd) 과정을 실시간으로 포착하여, ELISA가 최대 43배까지 과소평가하던 평형 해리 상수(KD)를 정확하게 산출해냅니다.
1. 바이오센서 진화 역사: 효소 전극에서 지능형 시스템까지
바이오센서의 역사는 1962년 Clark와 Lyons가 포도당 산화효소를 이용한 최초의 효소 전극을 개발하면서 시작되었습니다. (Clark & Lyons, 1962) 이후 1980년대 상용화된 혈당 모니터링 시스템은 일반인들도 바이오센서의 혜택을 누리게 한 결정적 계기가 되었습니다.
주요 발전 단계
- 1960s: 효소 기반 전기화학 센서의 탄생
- 1970-80s: ISFET 등 반도체 기반 BioFET의 등장 및 상용화
- 1990s: Biacore 시스템의 출시와 함께 SPR 기반의 실시간 분석 대중화
- 2020s+: AI 및 나노소재 통합, 웨어러블 및 고처리량(High-throughput) 어레이 진화
2. SPR vs ELISA: 왜 연구자들은 SPR로 이동하는가?
전통적인 ELISA 분석은 항원-항체 결합을 색상 변화로 측정하는 훌륭한 도구이지만, 연구 현장에서는 몇 가지 결정적인 한계에 부딪힙니다. 가장 큰 문제는 ‘종말점(End-point) 분석’이라는 점입니다. 이는 결합이 다 끝난 뒤의 결과만 보여줄 뿐, 얼마나 빠르게 결합하고 해리되는지는 알 수 없게 만듭니다.
| 분석 항목 | ELISA (전통 방식) | SPR (혁신 방식) |
|---|---|---|
| 분석 원리 | 효소-기질 색상 반응 | 플라즈몬 공명 각도 변화 |
| 레이블(표지) | 형광/효소 표지 필수 | 불필요 (Label-free) |
| 분석 시간 | 4-24시간 (다단계) | 실시간 (분 단위) |
| 검출 한계(LOD) | 약 1 ng/mL | 0.009 ~ 3.6 ng/mL |
| 동역학 정보 | 제공 불가 | ka, kd, KD 직접 산출 |
🔍 Deep Dive: 표지 방식보다 낮은 LOD의 비밀
ELISA는 발색 효소를 통한 ‘신호 증폭’ 과정이 있습니다. 하지만 왜 고감도 SPR이 더 낮은 검출 한계(LOD)를 보일까요?
- 배경 노이즈의 차이: ELISA는 발색 증폭 시 비특이적 결합으로 인한 배경 신호도 함께 커집니다. 반면, SPR은 마이크로플루이딕스 흐름 시스템을 사용하여 결합되지 않은 분자를 즉각 제거하므로 신호 대 잡음비(S/N Ratio)가 압도적으로 높습니다.
- 광학적 정밀도: 최신 Nano-SPRI 기술은 금박막 표면의 굴절률 변화를 PM(Pico-molar) 수준에서 검출할 수 있는 초정밀 CMOS 검출기를 사용합니다.
- 동적 데이터 분석: ELISA는 색이 변할 때까지 기다려야 하지만, SPR은 결합이 시작되는 초기 기울기(Rate)를 측정하므로 아주 적은 양의 분자가 결합하는 순간에도 정확한 농도를 역산할 수 있습니다.
*일반적인 SPR의 LOD는 nM 수준이나, 특정 고감도 시스템(예: Nano-SPRI)은 fM(Femto-molar) 수준까지 도달하여 ELISA의 한계를 뛰어넘습니다.
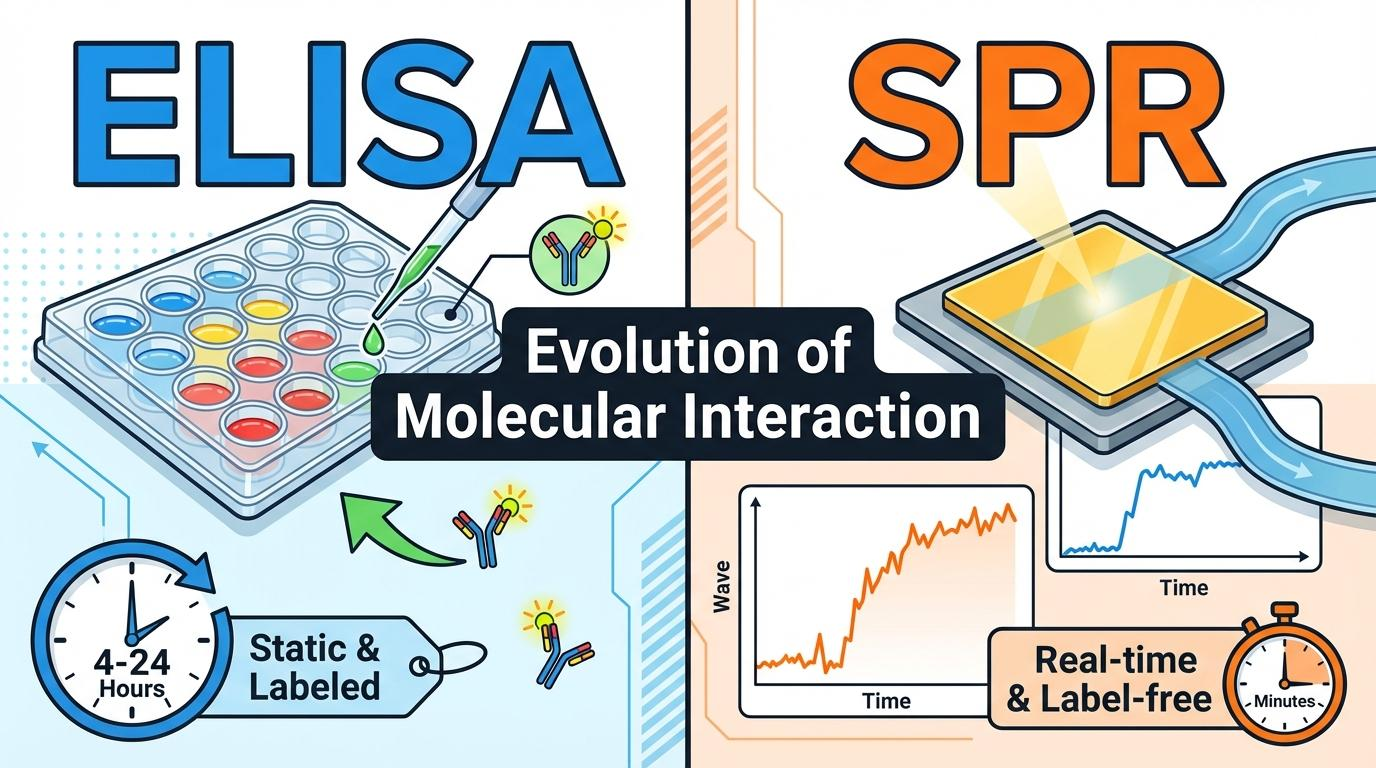
[그림 1] ELISA의 정적 분석과 SPR의 실시간 동역학 분석 비교
3. 바이오센서 발전의 정점, SPR의 작동 메커니즘
SPR 바이오센서는 금속 표면(주로 금박막)에서 발생하는 표면 플라즈몬 공명 현상을 이용합니다. 센서 표면에 시료가 결합하면 질량이 증가하고, 이로 인해 표면의 굴절률이 변하면서 반사되는 빛의 공명 각도가 이동합니다. 이를 통해 우리는 1 pg/mm2 수준의 아주 미세한 변화도 감지할 수 있습니다.
센서그램(Sensorgram)의 4단계
- Association(결합): 분석물이 리간드와 결합하며 반응 유닛(RU)이 상승하는 단계
- Equilibrium(평형): 결합과 해리 속도가 동일해져 곡선이 평탄해지는 단계
- Dissociation(해리): 버퍼 유동에 의해 결합체가 떨어져 나가며 RU가 감소하는 단계
- Regeneration(재생): 표면을 세척하여 다음 실험을 위해 리간드만 남기는 단계
4. 바이오센서의 미래: AI와 웨어러블의 융합
2025년 이후 바이오센서 시장은 연평균 9.5%의 성장을 거듭하여 2030년 약 543억 달러 규모에 이를 전망입니다. 특히 AI 딥러닝을 활용한 노이즈 제거 기술은 기존 하드웨어의 검출 한계를 100배 이상 개선하고 있으며, 나노로봇과 결합한 체내(In-vivo) 실시간 감지 기술이 상용화를 앞두고 있습니다.
📚 핵심 용어 정리 (Glossary)
- • KD (Equilibrium Dissociation Constant)
- 평형 해리 상수. 수치가 낮을수록 결합 친화도가 높음을 의미합니다.
- • ka (Association Rate Constant)
- 결합 속도 상수. 두 분자가 얼마나 빨리 결합하는지를 나타냅니다.
- • RU (Response Unit)
- SPR에서 측정되는 신호 단위. 1 RU는 센서 표면 질량 변화 약 1 pg/mm2에 해당합니다.
- • Label-free (비표지)
- 형광이나 효소 같은 별도의 표지 물질 없이 분자 본연의 특성을 이용해 검출하는 방식입니다.
자주 묻는 질문 (FAQ)
Q1. ELISA 데이터가 있는데 굳이 SPR을 또 해야 하나요?
A1. 신약 개발이나 정밀 분석 단계라면 필수입니다. ELISA는 KD 값을 과소평가하는 경향이 있으며, 약물의 효능을 결정짓는 ‘해리 속도(Residence time)’ 데이터를 제공하지 못하기 때문입니다.
Q2. SPR은 비용이 너무 비싸지 않나요?
A2. 초기 장비 도입 비용은 높지만, 레이블링 시약 비용이 들지 않고 센서 칩을 재생하여 수십 번 재사용할 수 있어 장기적인 운영 비용(OpEx) 면에서는 효율적일 수 있습니다.
문의 QR 코드 (메시지 연결)