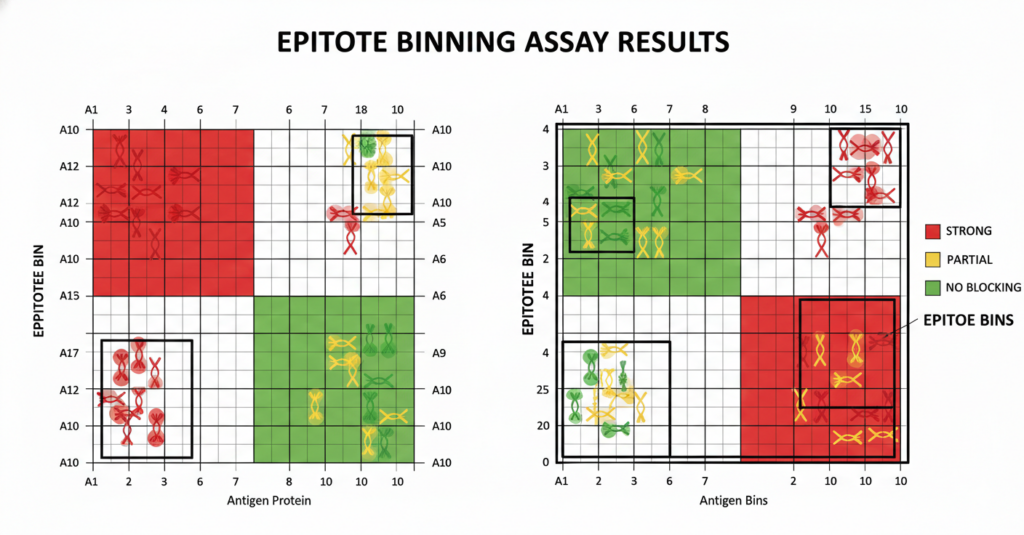
대량 단백질 생산의 성공은 단순한 세포 농도 증대를 넘어 수율 극대화와 기능성 유지라는 두 마리 토끼를 잡는 데 있습니다. 이를 위해 업스트림 공정에서 퍼퓨전(Perfusion)과 같은 고효율 배양 모드를 선택하고, SPR(Surface Plasmon Resonance) 분석을 통해 생산 단계별로 단백질의 결합 특성과 구조적 동질성을 실시간으로 검증하는 것이 바이오 공정 최적화의 핵심입니다.
1. 대량 단백질 생산 배양 조건: 왜 정교한 설계가 필요한가?
바이오 의약품 시장이 급성장함에 따라 항체 및 치료용 당단백질의 단백질 대량 생산 요구가 그 어느 때보다 높습니다. 하지만 연구 현장에서는 실험실 규모(Lab-scale)의 성공이 산업 규모(Production-scale)로 이어지지 않는 ‘스케일업 재현성’ 문제에 자주 직면합니다.
잘못된 대량 단백질 생산 배양 조건은 세포 사멸을 가속화할 뿐만 아니라, 단백질의 당쇄 패턴(Glycosylation)을 변화시켜 약물의 효능과 안전성에 치명적인 영향을 미칩니다. 따라서 단순한 증식이 아닌, 단위 부피 및 시간당 기능성 단백질의 수율을 극대화하는 전략적 접근이 필수적입니다.
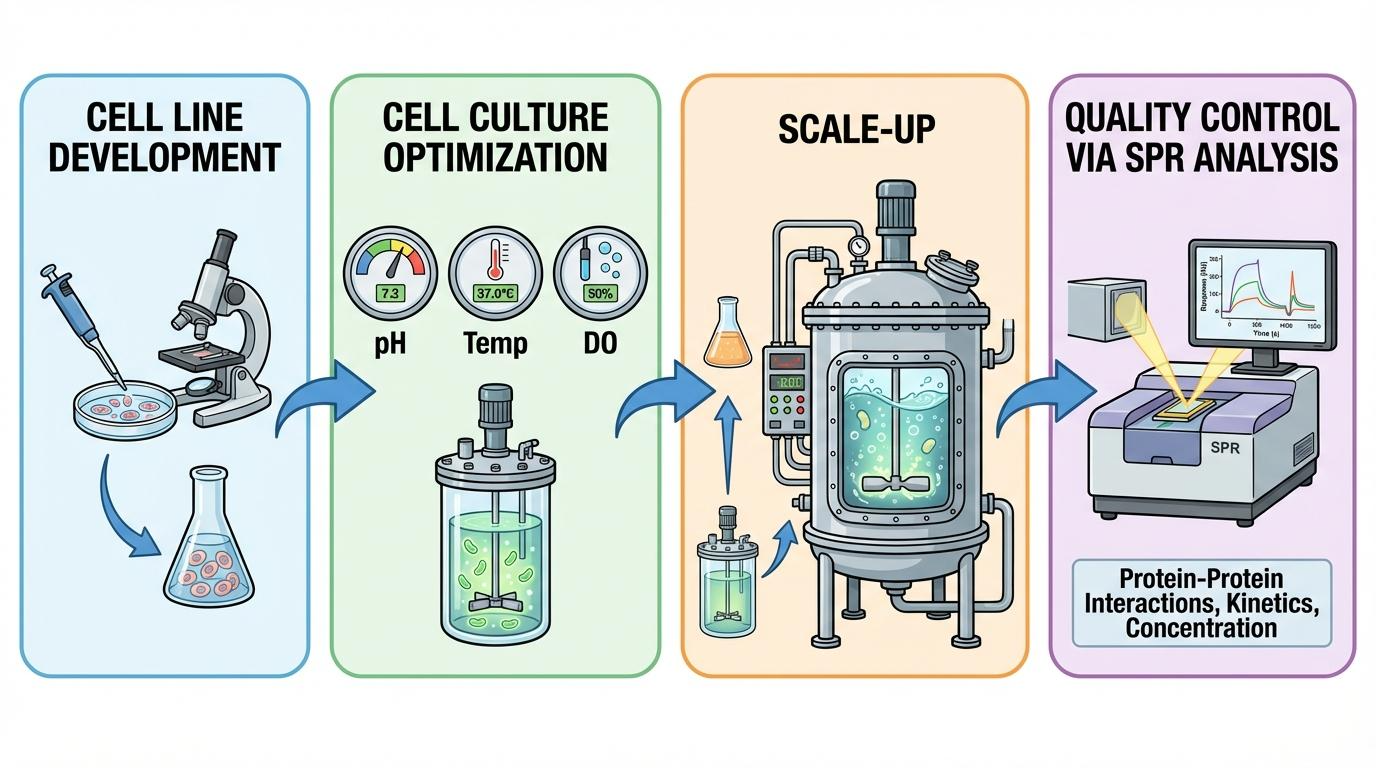
[인포그래픽: 업스트림 바이오 공정 최적화의 단계별 흐름]
2. 바이오 공정 최적화: 업스트림 전략의 핵심
성공적인 바이오 공정 최적화를 위해서는 공정 모드의 선택과 배지 최적화가 선행되어야 합니다. 특히 최근에는 기존 회분식 배양의 한계를 극복하기 위한 다양한 시도가 이루어지고 있습니다.
배양 모드별 성능 비교
| 공정 구분 | 특징 | 생산성 수치 예시 |
|---|---|---|
| 회분 (Batch) | 단순함, 짧은 배양 기간 | 기준 (1x) |
| 피드배치 (Fed-batch) | 부족 성분 공급, 세포 농도 향상 | 회분 대비 약 5~10배 |
| 퍼퓨전 (Perfusion) | 고농도 장기 유지, 노폐물 즉시 제거 | 회분 대비 50배 이상 향상 보고[2] |
Biphasic Culture 전략을 활용해 보세요. 성장기(37도)와 생산기(33-35도)를 분리하여 온도를 조절하면 세포 사멸을 늦추고 최종 단백질 농도를 20% 이상 끌어올릴 수 있습니다.
3. 세포 배양 조건 확립: 4대 핵심 파라미터
정교한 세포 배양 조건 확립을 위해 제어해야 할 물리·화학적 환경 수치는 다음과 같습니다.
- ✔ 온도(Temperature): 37도가 기본이나, 33-37도 범위 내 조절을 통해 단백질 생산성(Specific productivity)을 향상시키는 사례가 많습니다.
- ✔ pH 조절: 일반적으로 7.2-7.4 범위를 유지하며, CO2 농도와 중탄산염 시스템을 통해 안정화합니다.
- ✔ 용존산소(DO): 30-40% 수준이 권장되며, 50% 이상의 과도한 DO는 산화 스트레스를 유발하여 세포 생존율을 낮출 수 있습니다.
- ✔ 세포 밀도: 퍼프루전 공정의 경우 1×107 cells/mL 이상의 고농도 유지가 가능해야 경제성을 확보할 수 있습니다.
4. SPR 분석: 배양 생성물 단백질 품질 검증 전략
배양 조건이 변경될 때마다 생산된 단백질의 기능적 동질성을 확인하는 것은 필수적입니다. 저분자 분석과 달리, 배양 단백질(Large Molecule) 분석에서는 물질 전달 제한(MTL)을 방지하고 응집체에 의한 노이즈를 제어하는 것이 핵심입니다.
배양 단백질 분석을 위한 SPR 신뢰성 체크리스트
- 최적 고정화 밀도(Rmax 제어): 단백질 분석 시에는 500-1,000 RU 수준의 적정 밀도로 고정화하여, 과도한 결합에 의한 물질 전달 제한(MTL) 및 입체 장애(Steric hindrance)를 방지합니다.
- 배양 생성물(Analyte) 전처리: 배양 상등액 내의 세포 부스러기 및 단백질 응집체 제거를 위해 0.22 um 필터링과 14,000-16,000 g(4℃) 원심분리를 반드시 수행합니다.
- 버퍼 매칭(Buffer Matching): 분석 단백질 샘플을 SPR Running Buffer와 동일한 조성(pH, 이온 강도)으로 희석/교체하여 비특이적 흡착(NS)과 벌크 효과(Bulk Effect)를 최소화합니다.
- 농도 시리즈 설계: 예상 해리 계수(KD)를 중심으로 5-7개의 농도 구배(0.1x~10x KD)를 설정하여 결합 및 해리 곡선의 피팅 정확도를 높입니다.
핵심 용어 정리 (Glossary)
- Upstream Process (업스트림 공정)
- 세포주 개발부터 세포 배양 및 수확까지의 단백질 생산 초기 단계를 의미합니다.
- MTL (Mass Transport Limitation)
- SPR 분석 시 리간드 밀도가 너무 높거나 흐름 속도가 느려, 결합 속도가 실제 반응 속도가 아닌 확산 속도에 의해 제한되는 현상입니다.
- RU (Resonance Unit)
- SPR 분석에서 표면에 결합된 물질의 양을 나타내는 단위로, 1 RU는 약 1 pg/mm2의 단백질 양에 해당합니다.
자주 묻는 질문 (FAQ)
Q1. 대량 생산 시 가장 권장되는 배양 모드는 무엇인가요?
A1. 목적에 따라 다르지만, 최근 항체 생산에서는 퍼퓨전(Perfusion) 방식이 각광받고 있습니다. 초기 설비 투자는 높지만, 배양 기간 동안 신선한 배지를 지속적으로 공급하여 고농도의 세포를 장기간 유지할 수 있어 최종 생산성이 압도적으로 높기 때문입니다.
Q2. 배양 단백질 SPR 분석에서 전처리가 왜 중요한가요?
A2. 배양액에는 단백질 외에도 지질, 핵산, 응집체 등 다양한 불순물이 포함되어 있습니다. 이러한 성분들이 센서 칩 표면에 비특이적으로 결합하거나 미세 유로를 막으면 데이터의 신뢰성이 급격히 떨어지므로, 정밀한 원심분리와 필터링이 선행되어야 합니다.
더욱 정교한 바이오 공정 설계와 SPR 분석 최적화가 필요하신가요?
바이오 공정 분석 컨설팅 문의하기문의 QR 코드 (메시지 연결)