성공적인 재조합 단백질 생산 서비스 활용을 위해서는 단백질의 가용성과 정제 효율을 결정하는 His-tag, MBP-tag 등의 전략적 선택이 필수적입니다. 특히 막단백질(Membrane Protein)과 같은 난치성 타겟은 포유류 세포 시스템(CHO/HEK293)과 특수 소포화제 스크리닝이 수율을 좌우하며, 국내외 전문 CRO를 통해 평균 2~6주 내에 고순도 단백질 확보가 가능합니다.
주요 키워드: 재조합 단백질, His-tag, MBP-tag, 막단백질 정제, 바이오 CRO, 단백질 발현
재조합 단백질 발현 및 정제의 난제: 생산 효율을 떨어뜨리는 주요 원인
바이오 의약품 및 기초 연구의 핵심인 재조합 단백질 생산 시, 많은 연구원이 불용성 침전(Inclusion Body)과 단백질 분해(Degradation) 문제로 고심합니다. 특히 벤처 기업이나 대학원 실험실에서 고난도의 막단백질을 직접 생산하려 할 때, 최적화되지 않은 정제 공정은 연구 전체의 타임라인을 수개월 이상 지연시키는 리스크가 됩니다.
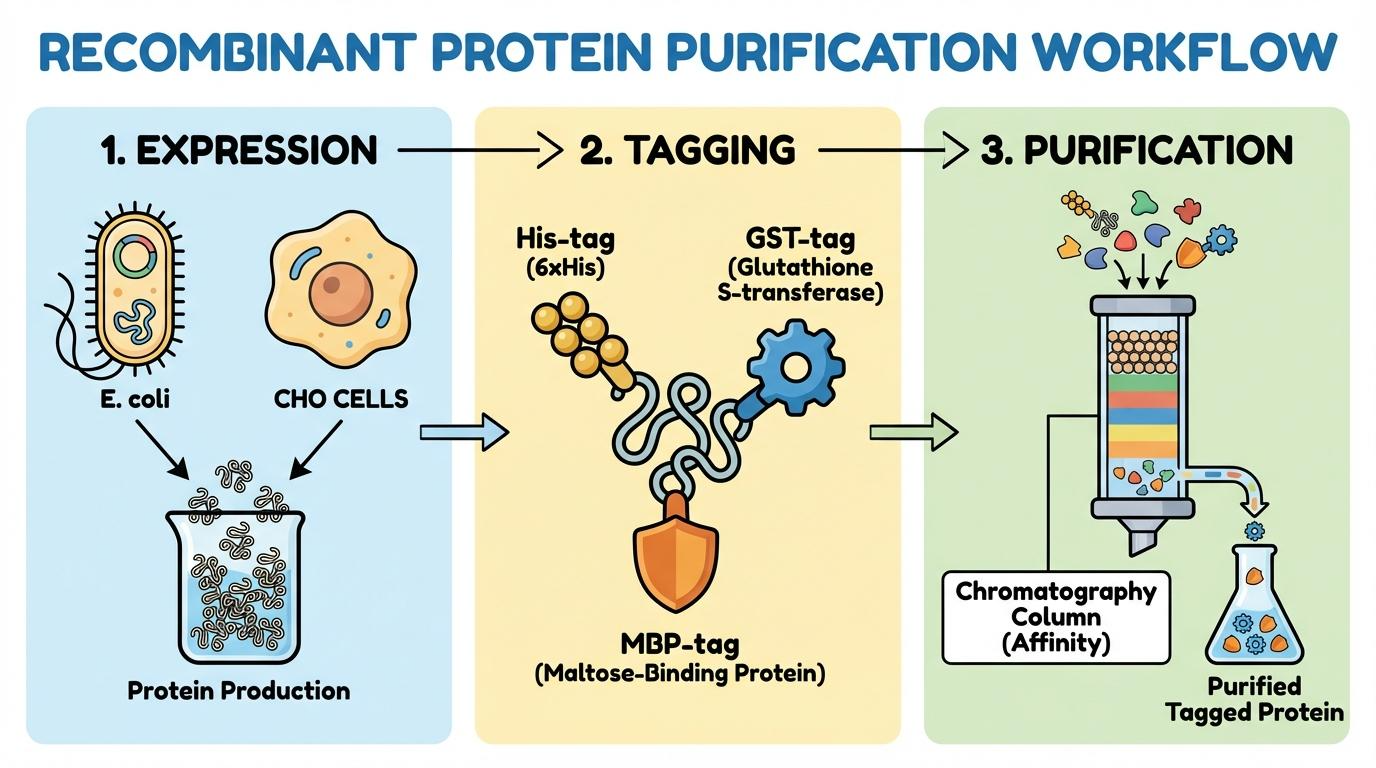
[그림 1] 단백질 발현 시스템 선택부터 태그 제거까지의 표준 공정 단계
1. 재조합 단백질 용해도 및 정제 수율을 결정하는 His-tag, MBP-tag 전략 가이드
단백질의 물리화학적 특성에 따라 적절한 태그를 부착하는 것은 발현량 증가와 정제 난이도 하락의 핵심입니다. 태그의 크기와 특성을 고려하여 N-말단 또는 C-말단 위치를 최적화해야 합니다.
| 태그(Tag) 종류 | 크기(kDa) | 주요 기능 및 장점 | 주의 사항 |
|---|---|---|---|
| His-tag (6xHis) | < 1.0 | 가장 보편적임, Ni-NTA 수지 정제 용이 | 비특이적 결합 가능성, 이미다졸 용출 |
| MBP-tag | ~40.0 | 가용성(Solubility) 비약적 향상 | 큰 크기로 인해 활성 저해 시 제거 필수 |
| GST-tag | ~26.0 | 이량체 형성 유도, 온화한 조건 정제 | 단백질 구조 및 활성에 영향 가능성 |
| SUMO-tag | ~12.0 | 접힘(Folding) 보조, 말단 정확한 절단 | 특이적 SUMO Protease 사용 필요 |
2. 막단백질(Membrane Protein) 발현 성공을 위한 Detergent 및 생산 최적화 실무 팁
막단백질은 소수성 도메인으로 인해 수용액 상에서 응집되기 매우 쉽습니다. 성공률을 높이기 위해서는 다음과 같은 정교한 조건 설정이 필요합니다.
🚀 실무 전문가의 Pro-tip: 막단백질 생산 파라미터
- 저온 발현 전략: 37°C 대신 16~20°C에서 발현하여 단백질 응집 속도를 늦추세요.
- 유도제 최적화: IPTG 0.1mM 이하의 낮은 농도로 유도하여 세포 내 스트레스를 줄입니다.
- 소포화제 스크리닝: DDM, LMNG 등 최소 10종 이상의 Detergent를 0.5~2% 농도 범위에서 테스트하여 안정성을 확보하십시오.
- 지질 환경 모방: 나노디스크(Nanodisc) 기술을 적용하면 단백질의 천연 구조와 활성을 70% 이상 보존할 수 있습니다.
국내외 맞춤형 재조합 단백질 생산 CRO 업체별 특성 및 정제 서비스 비교
연구 타임라인을 단축하고 고품질의 데이터를 확보하기 위해 검증된 CRO 인프라를 활용하는 것은 영리한 전략입니다. 특히 수도권 연구자들이 선호하는 주요 업체들의 특징을 정리했습니다.
GenScript (수원/경기)
시스템: TurboCHO, Expi293
특징: AI 코돈 최적화, 5일 내외의 초고속 발현, mg에서 kg 단위까지 대량 생산 지원.
Koma Biotech (서울)
시스템: CHO, HEK293, E.coli
특징: 막단백질 및 고난도 타겟 특화, 정제 조건 최적화 경험 풍부, 4~6주의 안정적 턴어라운드.
Y-bio Service (대전)
시스템: ExpiCHO/HEK, 효모
특징: 항원 및 연구용 단백질 소량 생산 시 합리적인 비용, 2~4주의 빠른 피드백.
재조합 단백질 생산 관련 자주 묻는 질문 (FAQ)
Q1. 단백질 정제 후 사용된 태그(Tag)를 반드시 제거해야 하나요?
A: His-tag(6xHis)처럼 크기가 매우 작은 태그는 대부분의 결합 실험이나 구조 분석에 지장을 주지 않습니다. 하지만 MBP-tag나 GST-tag처럼 큰 태그는 단백질의 고유 활성 부위를 가릴 수 있으므로, Protease(TEV, Thrombin 등) 사이트를 삽입하여 제거하는 것을 권장합니다.
Q2. E.coli 시스템과 포유류 세포(Mammalian) 시스템 중 무엇을 선택해야 할까요?
A: 당쇄화(Glycosylation)와 같은 번역 후 조절(PTM)이 단백질 활성에 핵심적이라면 CHO/HEK293와 같은 포유류 세포를 선택해야 합니다. 단순한 구조의 도메인이나 대량의 항원이 목적이라면 비용이 저렴한 E.coli 시스템이 유리합니다.
바이오 연구 핵심 용어 사전 (Glossary)
- Ni-NTA: Histidine 태그와 강하게 결합하는 니켈 이온 수지로, 친화성 크로마토그래피의 핵심 재료입니다.
- Inclusion Body: 대장균 내에서 단백질이 비정상적으로 뭉쳐 형성된 불용성 입자로, 리폴딩(Refolding) 공정이 필요합니다.
- Codon Optimization: 발현 숙주가 선호하는 코돈으로 서열을 교체하여 번역 속도를 높이는 기술입니다.
- PTM (Post-Translational Modification): 단백질 합성 후 일어나는 구조적 변형 과정으로 단백질의 기능과 안정성에 중요합니다.
참고문헌 및 출처:
- 1. GenScript, “Recombinant Protein Services & Expression Guide”, 2024.
- 2. Koma Biotech, “Advanced Protocols for Membrane Protein Purification”, 2023.
- 3. DBpia, “융합 태그를 이용한 단백질 용해도 및 발현 효율 최적화 연구”, Vol. 145.
※ 본 포스팅에 언급된 업체명(GenScript, Koma Biotech 등)은 각 해당 기업의 등록 상표이며, 본 콘텐츠는 학술 정보 공유 및 공공 연구 가이드를 목적으로 작성되었습니다.
문의 QR 코드 (메시지 연결)



