[SPR 분석] Affinity를 넘어 Avidity로: 항체 약효 예측의 새로운 기준
바이오 의약품 시장의 고도화에 따라, 연구실의 연구원들은 더욱 정교한 결합 분석 데이터를 필요로 하고 있습니다. 우리는 흔히 SPR 분석을 통해 단일 결합 세기인 Affinity(KD)를 측정하곤 합니다. 그러나 인비트로(In-vitro) 실험에서 우수한 KD 값을 보였던 후보 물질이 실제 세포 수준에서 효능을 발휘하지 못하는 “Affinity의 함정”은 연구 과정에서 흔히 발생하는 문제입니다.
“Affinity는 결합의 시작일 뿐,
실제 효능의 완성은 Avidity가 결정합니다.”
실제 효능의 완성은 Avidity가 결정합니다.”
현재 연구의 문제점: 왜 Affinity만으로는 부족한가?
세포 표면의 항원(Epitope)은 고밀도로 배열되어 있거나 클러스터를 형성하고 있습니다. 실제 항체는 두 개의 팔(Bivalent)을 활용해 다가성(Multivalent) 결합을 형성하며, 이때 발생하는 재결합(Rebinding) 효과는 단순히 1:1 모델로 설명할 수 없습니다. 연구의 정확도를 높이기 위해서는 결합의 양적인 수치를 넘어 질적인 구조를 파악해야 합니다.
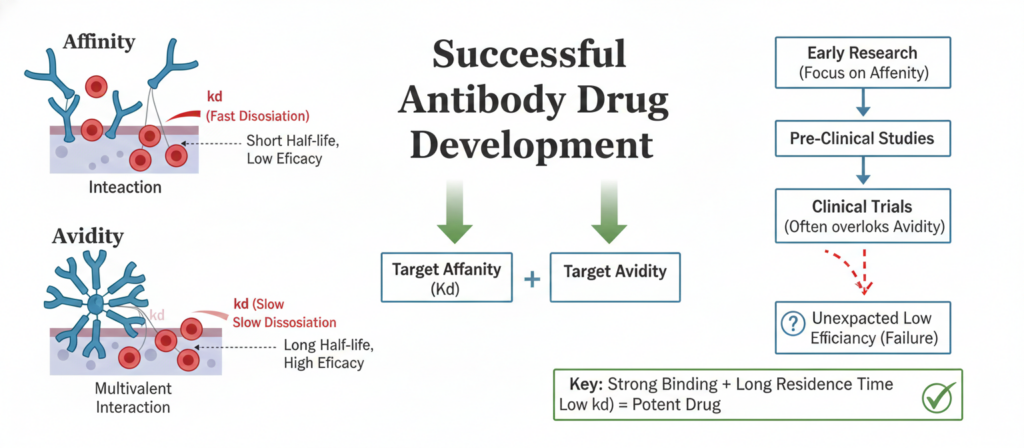
1. Affinity (결합 친화도)
단일 결합 부위 사이의 순수한 물리적 결합 세기. 1:1 상호작용의 상수를 기반으로 분석합니다.
2. Avidity (총 결합력)
여러 결합 부위가 동시에 관여하여 나타나는 누적 결합 강도. 구조적 지오메트리 효과가 포함됩니다.
해결방안: SPR 분석을 통한 Avidity 정밀 측정
성공적인 항체 개발의 목표는 ‘생체 내 환경에서의 약효 예측’입니다. 이를 위해 SPR 기술을 활용하여 리간드 밀도 제어와 유속 변화를 통해 Avidity 효과를 정량적으로 분석하는 것이 필수적입니다.
SPR 분석에서 Avidity가 수행하는 핵심 역할
- 다가성 효과(Multivalency) 측정: 항체가 타겟에 두 팔로 결합했을 때의 Residence Time(체류 시간)을 정밀 추적합니다.
- 항원 밀도 시뮬레이션: 세포 표면 항원 밀도에 따른 결합 효율을 예측하여 최적의 치료 농도를 도출합니다.
- Rebinding 분석: 해리된 항체가 다시 결합하는 과정을 수치화하여 생체 내 지속성을 과학적으로 입증합니다.
“고밀도 타겟 환경에서 Avidity를 간과하면,
최고의 후보 물질을 놓치게 됩니다.”
최고의 후보 물질을 놓치게 됩니다.”
Avidity 분석으로 얻는 연구 성과와 가치
SPR 기반의 Avidity 측정을 통해 연구자는 다음과 같은 차별화된 결과물을 얻을 수 있습니다.
- 임상 리스크 최소화: 세포 수준 효능과 높은 상관관계를 가진 데이터를 확보하여 선별 과정의 불확실성을 제거합니다.
- PK/PD 모델링 고도화: 매우 느린 Apparent koff 값을 분석하여 정교한 약물 투여 스케줄링이 가능해집니다.
- 변이 대응 전략 수립: 돌연변이 타겟에 대해서도 Avidity 덕분에 유지되는 기능적 안정성을 정량화할 수 있습니다.
참고 문헌
- Motsa, B. B. (2023). A beginner’s guide to surface plasmon resonance. The Biochemist, 45(1), 1–6.
- Schuck, P., & Zhao, H. (2010). The Role of Mass Transport Limitation and Surface Heterogeneity in the Biophysical Characterization of Macromolecular Binding Processes by SPR Biosensing. Methods in Molecular Biology, 627, 15–54.
- Errington, W. J., Bruncsics, B., & Sarkar, C. A. (2019). Mechanisms of noncanonical binding dynamics in multivalent protein–protein interactions. PNAS, 116(51), 25659–25667.
- Schasfoort, R. B. M. (2023). Gradient method for accurate affinity determinations. Analytical Biochemistry, 667, 115085.