SPR 분석의 데이터 안정성을 확보하려면 단순한 고착이 아닌 전략적 고정화(Immobilization)가 선행되어야 합니다. 데이터 품질을 결정하는 핵심은 SPR 분석 고정화 최적화 전략을 통해 리간드의 활성을 유지하면서 적절한 밀도(50~300 RU)와 방향성을 설계하는 데 있습니다. 특히 pH Scouting을 통해 최적의 농축 조건을 찾고, 실험 목적(Kinetics vs Screening)에 맞는 고정화 방식을 선택하는 것이 성공의 열쇠입니다.
SPR 데이터가 흔들리는 이유: 왜 고정화가 문제인가?
많은 연구자들이 SPR 분석 시 결합 신호(Binding Signal)가 낮거나 재현성이 떨어지는 문제로 고민합니다. 대개 분석 물질(Analyte)의 문제라고 생각하기 쉽지만, 실제 원인은 Immobilization 최적화 실패에 있는 경우가 많습니다. 리간드가 칩 표면에 너무 빽빽하게 붙어 질량 전달 제한(Mass Transport Limitation)이 발생하거나, 무작위 방향으로 고정되어 활성 부위가 가려지면 데이터 피팅은 왜곡될 수밖에 없습니다.
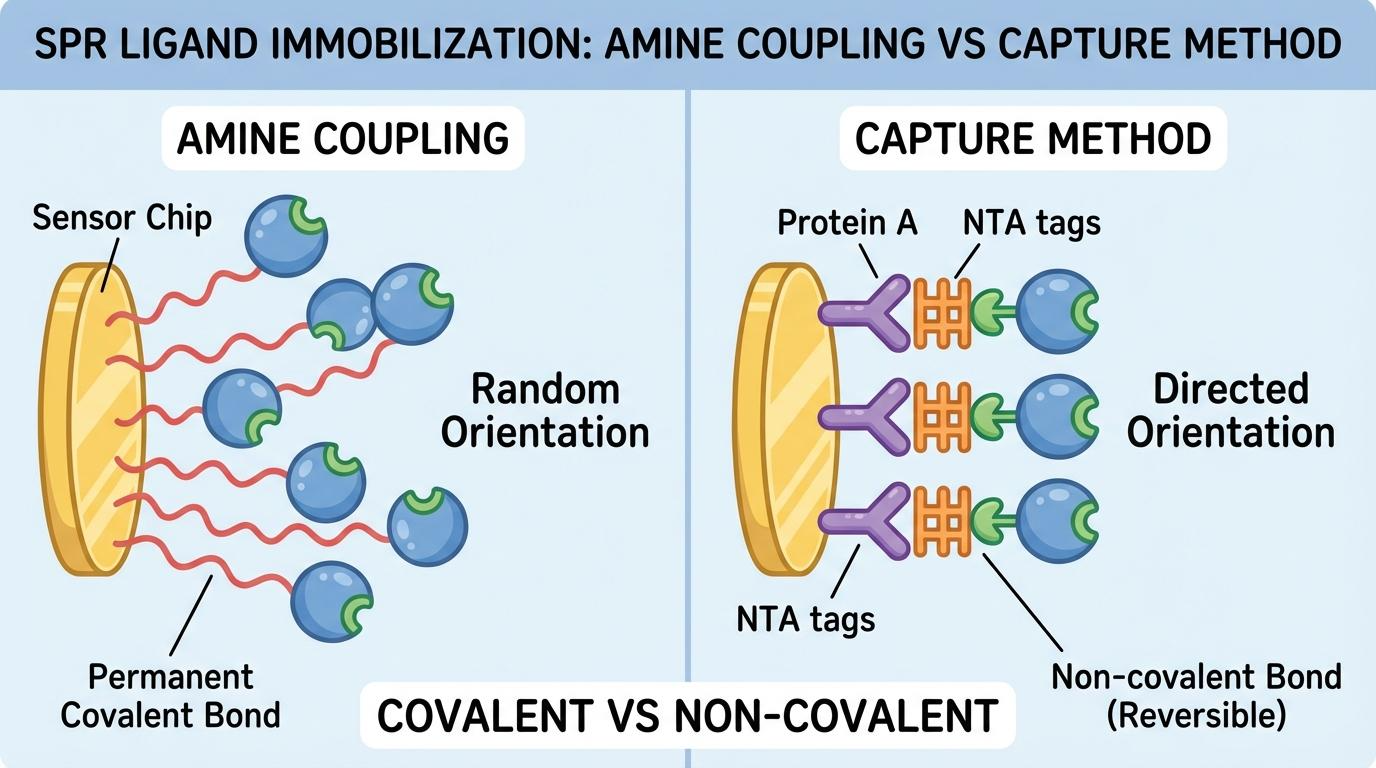
[그림 1] 고정화 방식에 따른 리간드 배치와 데이터 품질의 차이
1단계: 센서 칩 준비와 표면 처리의 핵심
성공적인 분석은 리간드의 화학적 특성과 센서 칩 준비 단계를 일치시키는 것에서 시작합니다. SPR 표면 처리의 목적은 비특이적 결합을 최소화하면서 리간드 접근성을 높이는 것입니다.
- CM5 (COOH 기반): 가장 범용적인 3D 매트릭스 칩으로 아민 커플링에 최적화되어 있습니다.
- NTA/Biotin 기반: 특정 태그(His-tag, Biotin)가 있는 리간드를 일정한 방향으로 잡을 때 유리합니다.
- 2D 표면 vs 3D 표면: 분자량이 큰 물질이나 복합체 분석 시 3D 매트릭스의 입체적 방해를 고려하여 2D 칩을 선택하기도 합니다.
2단계: pH Scouting – “잘 붙는 pH”가 아닌 “건강한 pH” 찾기
리간드를 칩 표면으로 끌어당기기 위해서는 정전기적 농축이 필요합니다. 리간드의 등전점(pI)보다 약 0.5~1.0 낮은 pH 버퍼를 사용하면 리간드는 (+) 전하를, 칩 표면은 (-) 전하를 띠게 되어 농축이 일어납니다.
3단계: 고정화 전략 선택 (Amine Coupling vs Capture)
실험 목적에 따라 공유결합인 Amine Coupling을 쓸지, 비공유결합인 Capture 방식을 쓸지 결정해야 합니다.
| 비교 항목 | Amine Coupling (공유결합) | Capture 방식 (비공유결합) |
|---|---|---|
| 결합 형태 | 공유결합으로 영구 고정 | 비공유결합 기반의 선택적 포획 |
| 리간드 방향성 | 무작위 (Random) | 일정함 (Directed) |
| 표면 안정성 | 매우 높음 | 상대적으로 낮음 (매 사이클 관리) |
| 추천 대상 | Tag 없는 단백질, 저분자 화합물 | 항체, His-tag 단백질 |
4단계: 밀도와 Rmax 설계 수치 가이드
Kinetics 분석에서 가장 흔한 실수는 리간드를 너무 많이 붙이는 것입니다. 고밀도 고정은 질량전달 제한(Mass Transport Limitation)과 비특이적 결합을 유발합니다.
- 저밀도 권장량: 일반적으로 50~300 RU(Response Units) 수준의 고정화가 권장됩니다.
- 목표 Rmax 계산: 이론적 최대 반응량(Rmax)은 다음과 같이 계산합니다.
Rmax = (Analyte MW / Ligand MW) x RL x Valency
*RL: 고정화된 리간드 양(RU), Valency: 결합가수(보통 1)
예를 들어, 100 kDa 리간드에 10 kDa 분석 물질이 붙는다면, 500 RU의 리간드 고정 시 이론적 Rmax는 50 RU가 됩니다. 실제 실험에서는 Rmax가 30~100 RU 사이가 되도록 RL을 조절하는 것이 가장 안정적입니다.
5단계: 데이터 재현성 확보와 실무 체크리스트
벤처 팀장님들이나 연구원들이 데이터 신뢰성을 높이기 위해 반드시 확인해야 할 실전 리스트입니다.
✅ SPR 분석 고정화 최적화 체크리스트
- 리간드와 칩 표면 기능기의 화학적 궁합을 먼저 확인했는가?
- pH Scouting을 통해 활성이 유지되는 최저 pH를 찾았는가?
- Kinetics 목적에 맞게 저밀도(50~300 RU) 고정을 수행했는가?
- 방향성이 중요하다면 Capture 방식(Protein A/G 등)을 검토했는가?
- 재생(Regeneration) 조건이 리간드 층을 손상시키지 않는가?
핵심 용어 정리 (Glossary)
- Immobilization (고정화)
- SPR 센서 칩 표면에 리간드를 물리적/화학적으로 결합시키는 과정입니다.
- Response Unit (RU)
- SPR 신호의 단위로, 대략 1 pg/mm2의 질량 변화가 1 RU에 해당합니다.
- Mass Transport Limitation (질량 전달 제한)
- 분석 물질이 표면의 리간드와 결합하는 속도가 확산 속도에 의해 제한되어 데이터가 왜곡되는 현상입니다.
- Regeneration (재생)
- 결합된 분석 물질을 떼어내고 리간드를 다시 활성 상태로 되돌리는 과정입니다.
자주 묻는 질문 (FAQ)
Q1: Amine coupling 후 결합 신호가 전혀 없습니다. 무엇이 문제인가요?
A1: 리간드의 활성 부위(Binding Site)에 아민기가 포함되어 고정화 과정에서 부위가 막혔을 가능성이 큽니다. 이 경우 방향성을 조절할 수 있는 Capture 방식을 사용해 보십시오.
Q2: pH Scouting에서 pH 4.0이 가장 많이 붙는데 이 조건으로 실험해도 될까요?
A2: 아니요. 너무 낮은 pH는 단백질의 3차 구조를 파괴할 수 있습니다. 농축량이 조금 적더라도 단백질이 안정적인 pH 영역 중 가장 낮은 값을 선택하는 것이 좋습니다.
참고문헌
- YclueBio, “SPR Ligand Immobilization Strategy Guide” (2024).
- iCLUEBIO, “SPR Sensor Chip Immobilization & Surface Modification Guide”.
- Xantec Application Note 10, “Optimized Methods for Surface Immobilization”.
- PubMed, “Surface Plasmon Resonance Principle and Optimization” (2016).
* 본 포스팅에 언급된 상표권(CM5, BIAcore 등)은 해당 소유권자에게 있습니다. 본 가이드는 연구 및 정보 전달 목적으로 작성되었습니다.
문의 QR 코드 (메시지 연결)