핵심 요약:
성공적인 Biomolecular Interaction Analysis를 위해서는 SPR 실험 한계인 신호 왜곡의 3대 요인(비특이적 결합, 버퍼 불일치, 온도 변화)을 반드시 통제해야 합니다. 이러한 요인들은 굴절률(Bulk RI)의 변동을 일으켜 실제 결합 신호를 가리고 데이터의 과대평가를 유발하므로, Isothermal Titration Calorimetry (ITC)나 MicroScale Thermophoresis (MST)를 통한 교차 검증으로 데이터 신뢰성을 확보하는 것이 필수적입니다.
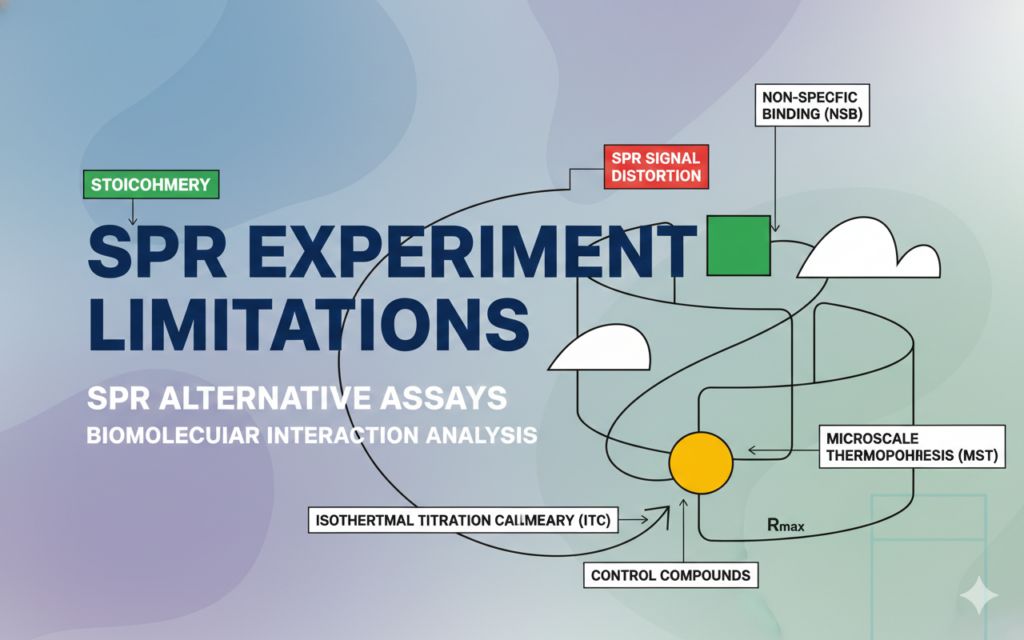
1. SPR 실험 한계와 신호 왜곡의 3대 핵심 요인
Biomolecular Interaction Analysis에서 SPR은 가장 강력한 도구이지만, 주변 환경 변화가 물리적인 굴절률 변동으로 이어지는 인과관계에 따라 데이터가 왜곡될 위험이 큽니다. 연구자가 반드시 통제해야 할 3가지 요소를 정리하면 다음과 같습니다.
- 버퍼 조성(Buffer Mismatch): 리간드가 고정된 칩 표면의 버퍼와 주입되는 분석물질의 버퍼 조성이 미세하게 다를 경우, 매우 민감한 굴절률(Bulk RI) 변화가 발생하여 분석 신호에 혼입됩니다.
-
온도 변화(Temperature Instability): SPR 센서는 온도의 미세한 요동에도 굴절률이 급격히 변동합니다. 이는 베이스라인의 드리프트(Drift)*를 유발하여 실제 신호의 높이를 왜곡시키는 주원인이 됩니다.
*주석: 베이스라인 드리프트(Baseline Drift)란 결합 반응과 상관없이 시간이 지남에 따라 센서 신호(RU)가 일정한 방향으로 서서히 상승하거나 하강하는 현상을 의미합니다.
-
비특이적 결합(NSB)에 의한 결합력 과대평가**: 분석 물질이 타겟 외의 빈 공간이나 칩 표면에 무분별하게 흡착되어 전체 RU 값을 인위적으로 높입니다.
**RU와 결합력의 상관관계:
SPR 소프트웨어는 측정된 RU 값을 리간드와 분석물질이 결합한 ‘질량’으로 인식합니다. 만약 NSB로 인해 RU 값이 실제보다 높게 측정되면, 분석 프로그램은 “낮은 농도에서도 이렇게 많이 결합하다니, 둘 사이의 친화력(Affinity)이 매우 강력하구나!”라고 판단하게 됩니다.
결과적으로 데이터가 실제보다 훨씬 낮은 농도에서 이미 최대 결합치에 도달(조기 포화)한 것처럼 피팅(Fitting)되며, 이로 인해 해리 상수(Kd) 값이 실제보다 낮게(즉, 결합력은 더 강하게) 산출되는 원인이 됩니다.
예시: 실제로는 100 nM 농도에서 50 RU만큼 붙어야 하는 샘플이, NSB 때문에 150 RU로 측정되었다면? 분석 프로그램은 이 물질을 100 nM만 줘도 엄청나게 잘 붙는 ‘슈퍼 바인더’로 오해하여, Kd 값을 실제보다 3~5배 더 강한 수치로 계산해 버립니다.
결론적으로, [버퍼/온도/NSB 변동] → [굴절률(RI) 변화 유도] → [분석 신호 혼입]의 순서로 SPR 신호 왜곡이 발생합니다.
2. SPR 대체 분석법 비교 전략: ITC 및 MST
SPR 신호 왜곡이 의심되거나 물리적 한계로 측정이 어려운 경우, Biomolecular Interaction Analysis의 신뢰성을 높여줄 전략적 대체 기술들을 활용해야 합니다.
| 비교 항목 | SPR (Kinetics 중심) | Isothermal Titration Calorimetry (ITC) | MicroScale Thermophoresis (MST) |
|---|---|---|---|
| 시료 상태 | 표면 고정 필요 | 완전 용액상 (Native) | 용액상 (표면 고정 불필요) |
| 주요 제공 정보 | kon, koff, Kd | Delta H, Delta S, n (Stoichiometry) | Kd (친화도 중심) |
| 왜곡 요인 대처 | RI 변화에 매우 민감 | 표면 고정 및 RI 아티팩트 없음 | 극소량 샘플로 NSB 영향 최소화 |
3. 데이터 신뢰성을 결정짓는 실무 가이드라인: Stoichiometry 검증
논문 투고 시 리뷰어가 가장 먼저 확인하는 것은 “이 실험 결과가 생물학적으로 타당한가?”입니다. 단순히 피팅 소프트웨어가 계산해준 값을 그대로 믿기보다, 아래의 기준을 통해 데이터의 물리적 개연성을 직접 검토해야 합니다.
💡 [대학원생 필독] Stoichiometry 및 데이터 검증 체크리스트
-
이론적 Rmax 계산 및 비교: 아래 공식을 통해 산출된 이론값과 실제 측정된 Rmax를 반드시 비교하세요.
Rmax, theoretical = (MW analyte / MW ligand) x R ligand x Valency측정된 Rmax가 이론값보다 현저히 높다면(예: 150% 초과), 이는 십중팔구 NSB(비특이적 결합) 또는 시료의 응집(Aggregation) 신호가 섞인 것입니다.
- 표면 활성도(Activity) 확인: 대조군 화합물(Known binder)을 주입했을 때 관측되는 Rmax가 이론값의 30% 미만이라면, 고정화 과정에서 단백질이 변성되었을 가능성이 큽니다. 이 경우 얻어진 Kd 값은 신뢰하기 어렵습니다.
- Isothermal Titration Calorimetry (ITC) 교차 검증: SPR의 1:1 모델에서 산출된 Stoichiometry(분자 간 결합 비) 값이 모호하다면, ITC를 통해 실제 결합 비가 1인지를 확인하십시오. 두 데이터의 일치성은 논문의 설득력을 2배 이상 높여줍니다.
4. 자주 묻는 질문 (FAQ)
Q1. 왜 SPR은 버퍼 차이에 그토록 민감한가요?
A. SPR의 측정 원리인 굴절률(RI)은 용액 내의 염 농도, DMSO 함량 등에 따라 선형적으로 변하기 때문입니다. 이러한 벌크 효과(Bulk effect)는 실제 결합보다 훨씬 큰 신호를 유발할 수 있습니다.
Q2. 온도 제어만 잘하면 신호 왜곡을 막을 수 있나요?
A. 온도는 베이스라인 안정성에 기여하지만, NSB나 버퍼 조성에 의한 왜곡은 별개의 문제입니다. 따라서 온도 제어와 함께 철저한 버퍼 매칭과 레퍼런스 채널 설계가 병행되어야 합니다.
5. 참고문헌
- Myszka, D. G. (1997). Kinetic analysis of macromolecular interactions using surface plasmon resonance biosensors. Current Opinion in Biotechnology, 8(1), 50-57.
- Schasfoort, R. B., & Tudos, A. J. (2017). Handbook of Surface Plasmon Resonance. Royal Society of Chemistry.
- SAGE Journals. (2020). Guidelines for High-Quality Surface Plasmon Resonance Data. SLAS Discovery.
- Elife Sciences. (2020). Avoiding Overinterpretation in Biosensor Experiments.
- Nicoya Life. (2024). Top 10 Tips for High-Quality SPR Data. Retrieved from https://nicoyalife.com/blog/spr-tips/