항체-분해약물접합체(DAC): ADC와 TPD의 한계를 넘는 차세대 항암 전략
신약 개발 연구자들이 겪는 가장 큰 고충 중 하나는 바로 ‘강력한 약효’와 ‘안전한 투여량’ 사이의 아슬아슬한 줄타기입니다. 특히 항암제 분야에서 치료지수(Therapeutic Index, TI)를 확보하지 못해 임상 단계에서 좌절되는 프로젝트는 부지기수입니다.
기존의 ADC(Antibody-Drug Conjugate)는 정밀 타격의 길을 열었지만 오프-타겟 독성(Off-target toxicity)에서 자유롭지 못했고, TPD(Targeted Protein Degradation)는 경구 투여 시 낮은 생체 이용률과 전신 노출 조절의 한계를 가졌습니다. 이 두 기술의 정수만을 결합한 DAC(Degrader-Antibody Conjugate)가 왜 차세대 바이오 모달리티의 주인공으로 떠오르는지, 와이클루바이오와 함께 분석해 보겠습니다.
- DAC = 항체(정밀 타격) + TPD(촉매적 분해): 단백질 기능을 억제하는 수준을 넘어 아예 분해하여 제거합니다.
- 치료지수(TI) 극대화: 적은 양으로도 반복적인 분해 작용을 수행하여 일반 세포 독성을 최소화합니다.
- 내성 극복: 기존 Inhibitor 방식의 한계인 변이 단백질에도 강력하게 대응할 수 있습니다.
1. 항체-분해약물접합체, DAC란 무엇인가?
항체-분해약물접합체(Degrader-Antibody Conjugate, DAC)는 항체에 세포 독성 항암제 대신 ‘단백질 분해제(Degrader)’를 결합한 형태입니다.
전통적인 ADC가 암세포 내로 독성 물질(Payload)을 전달하여 직접적으로 사멸시킨다면, DAC는 항체가 암세포를 인식해 내부로 진입한 후, 세포 내 유비퀴틴-프로테아좀 경로를 활성화하여 질환 유발 단백질을 선택적으로 분해합니다. 이는 마치 ‘유도 미사일’에 ‘표적 해체 도구’를 실어 보내는 것과 같습니다.
2. DAC의 등장 배경: 기존 기술의 ‘Pain Points’
– ADC의 한계: 페이로드의 강력한 독성으로 인해 안전하게 투여할 수 있는 용량 범위(TI)가 매우 좁습니다.
– TPD의 한계: 대사 과정에서 약물이 혈액 순환에 도달하는 비율인 ‘생체 이용률’이 낮고, 전신 노출 시 의도치 않은 부작용 조절이 어렵습니다.
| 비교 항목 | ADC | TPD (PROTAC 등) | DAC (Degrader-Antibody) |
|---|---|---|---|
| 작용 방식 | 세포 사멸 (직접 독성) | 단백질 분해 (경구/전신) | 표적 특이적 단백질 분해 |
| 특이성(Specificity) | 높음 (항체 기반) | 낮음 (전신 노출) | 최고 수준 (항체 유도) |
| 재사용성 | 1회성 작용 | 촉매적 반복 분해 | 촉매적 반복 분해 |
| 치료지수(TI) | 제한적 | 관리 필요 | 획기적 확장 가능 |
3. DAC의 기술적 장점: 왜 더 강력한가?
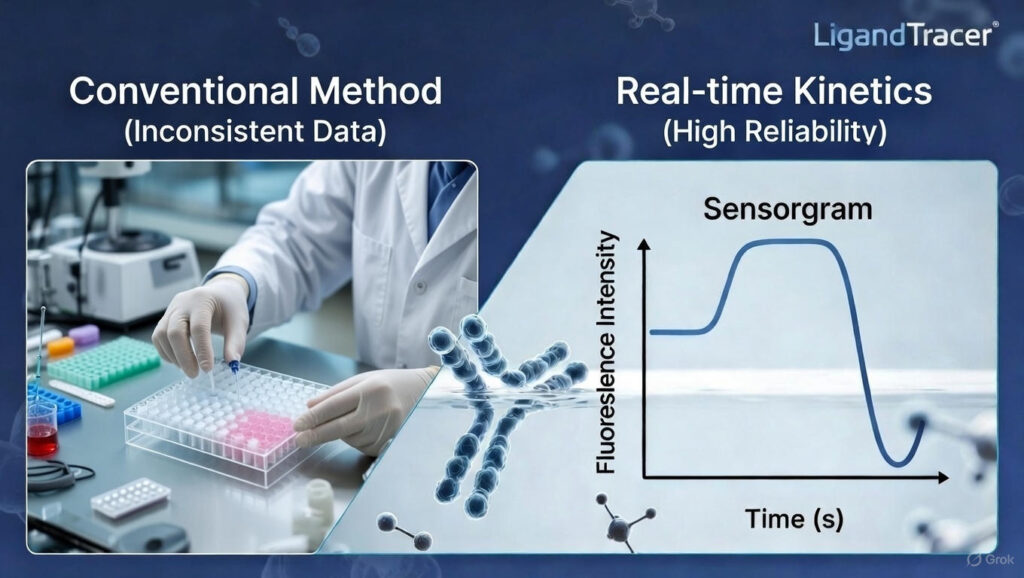
- 높은 특이성과 효율성: 항체의 SPR 분석이나 Binding Kinetics(ka, kd) 값을 최적화하여 타겟 세포에만 정확히 도달하게 함으로써 TPD의 강력한 파괴력을 집중시킵니다.
- 낮은 독성: 분해제는 ‘촉매’처럼 작용하여 한 분자가 여러 표적 단백질을 제거할 수 있습니다. 따라서 ADC보다 적은 양의 페이로드로도 충분한 항암 효과를 내며, 부작용은 줄어듭니다.
- 광범위한 적용성: 기존 억제제(Inhibitor)가 접근할 수 없었던 ‘Undruggable’ 타겟에도 적용 가능합니다.
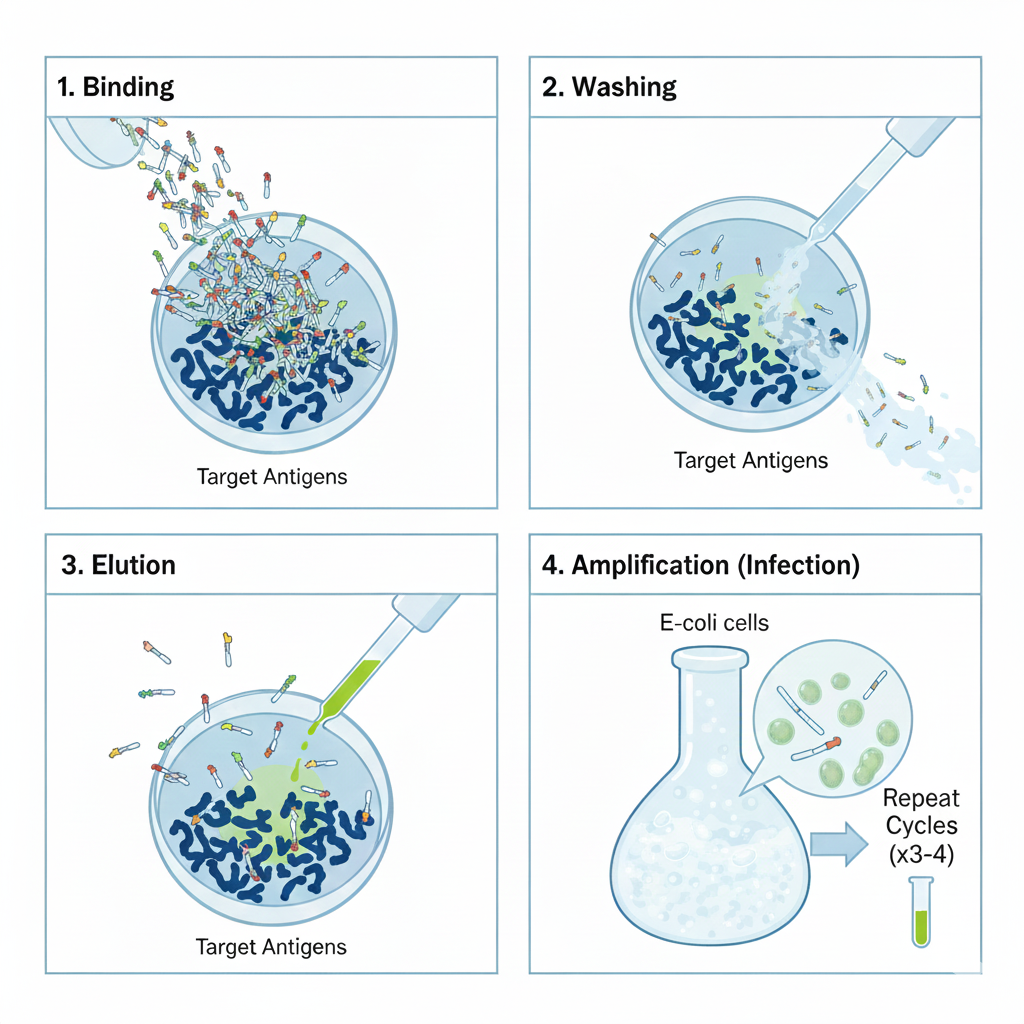
4. 작동 메커니즘 (Process)
DAC가 세포 내에서 작용하는 과정은 매우 정교하게 설계되어야 합니다.
5. 글로벌 개발 동향 및 주요 기업
이미 Roche(Genentech)가 2019년에 DAC 관련 핵심 논문을 발표하며 경쟁의 서막을 알렸습니다. 최근에는 빅파마들의 공격적인 투자가 이어지고 있습니다.
- Firefly Bio: 일라이 릴리 등으로부터 거액의 투자를 유치하며 DAC 전용 플랫폼 개발에 매진 중입니다.
- Nurix Therapeutics: 화이자(구 씨젠)와 파트너십을 맺고 고형암 타겟 DAC를 연구하고 있습니다.
- C4 Therapeutics: 머크(Merck)와 공동 개발을 통해 ‘TORPEDO’ 플랫폼 기반의 혁신 신약을 준비하고 있습니다.
6. Q&A: 항체-분해약물접합체(DAC) 심층 이해
정밀한 항체 분석과 신뢰도 높은 데이터가 필요하십니까?
와이클루바이오는 SPR, Binding Kinetics 분석부터 신규 항체 발굴까지,
여러분의 DAC 프로젝트 성공을 위한 최적의 기술 파트너가 되어 드립니다.