핵심 요약
Phage Display 항체 제작은 M13 박테리오파지의 유전적 조작을 통해 특정 항체를 파지 표면에 노출시켜 최적의 바인더를 선별하는 기술입니다. 이 기술은 유전형과 표현형을 직접 연결함으로써 109개 이상의 방대한 항체 라이브러리 구축을 가능하게 하며, 반복적인 바이오팬닝 공정을 통해 결합력이 극대화된 항체를 신속하게 발굴할 수 있습니다. 특히 M13 파지의 pIII 단백질 융합 시스템은 항체의 구조적 안정성을 유지하면서도 고효율의 스크리닝 환경을 제공합니다.
주요 키워드: Phage Display 항체 제작, M13 박테리오파지 원리, pIII 단백질, 바이오팬닝, 항체 라이브러리
1. 박테리오파지, 왜 바이러스가 Phage Display 항체 제작의 핵심이 되었을까요?
현대 바이오 의약품의 중추를 담당하는 항체 치료제 개발에서 가장 어려운 단계는 수많은 후보 물질 중 유효한 항체를 가려내는 것입니다. Phage Display 항체 제작 기술은 이러한 난제를 해결하기 위해 M13 박테리오파지의 독특한 생물학적 특성을 활용합니다.
M13 박테리오파지는 대장균을 숙주로 삼지만, 숙주 세포를 파괴하지 않고 지속적으로 증식하는 비용해성(Non-lytic) 특성을 가집니다. 이는 연구자가 원하는 항체 라이브러리를 손상 없이 대량으로 복제할 수 있는 최적의 환경을 제공합니다. 특히 단일 가닥 DNA(ssDNA) 구조 덕분에 외부 항체 유전자 삽입이 매우 용이하여, 이론적으로 1012 cfu/mL 이상의 고농도 파지 입자를 확보할 수 있습니다.
실제 벤처 연구 현장에서는 라이브러리의 다양성(Diversity)이 항체 발굴의 성패를 결정합니다. 유효한 스크리닝을 위해서는 최소 108에서 1010 사이의 독립적인 클론을 확보해야 하며, 이를 위해 대장균의 형질전환 효율을 극대화하는 전기천공법(Electroporation)이 주로 사용됩니다.
2. M13 박테리오파지 원리: pIII 단백질이 수행하는 역할은 무엇인가요?
M13 파지의 표면에는 여러 종류의 코트 단백질이 존재하지만, Phage Display 항체 제작에서 가장 널리 쓰이는 것은 pIII 단백질입니다. 이 단백질은 파지 입자의 말단에 3~5개 정도 존재하며, 대장균의 F-pilus에 부착하여 감염을 주도하는 핵심 부위입니다.
연구자들은 scFv 제작 시 항체의 가변 부위(VH, VL)를 연결한 유전자를 pIII 유전자와 융합시킵니다. 이렇게 조립된 파지는 자신의 머리 끝에 항체를 매달고 다니게 되며, 내부에는 해당 항체의 설계도인 DNA를 품고 있습니다. 이러한 유전형과 표현형의 물리적 연결이 바로 Phage Display의 혁신적인 원리입니다.
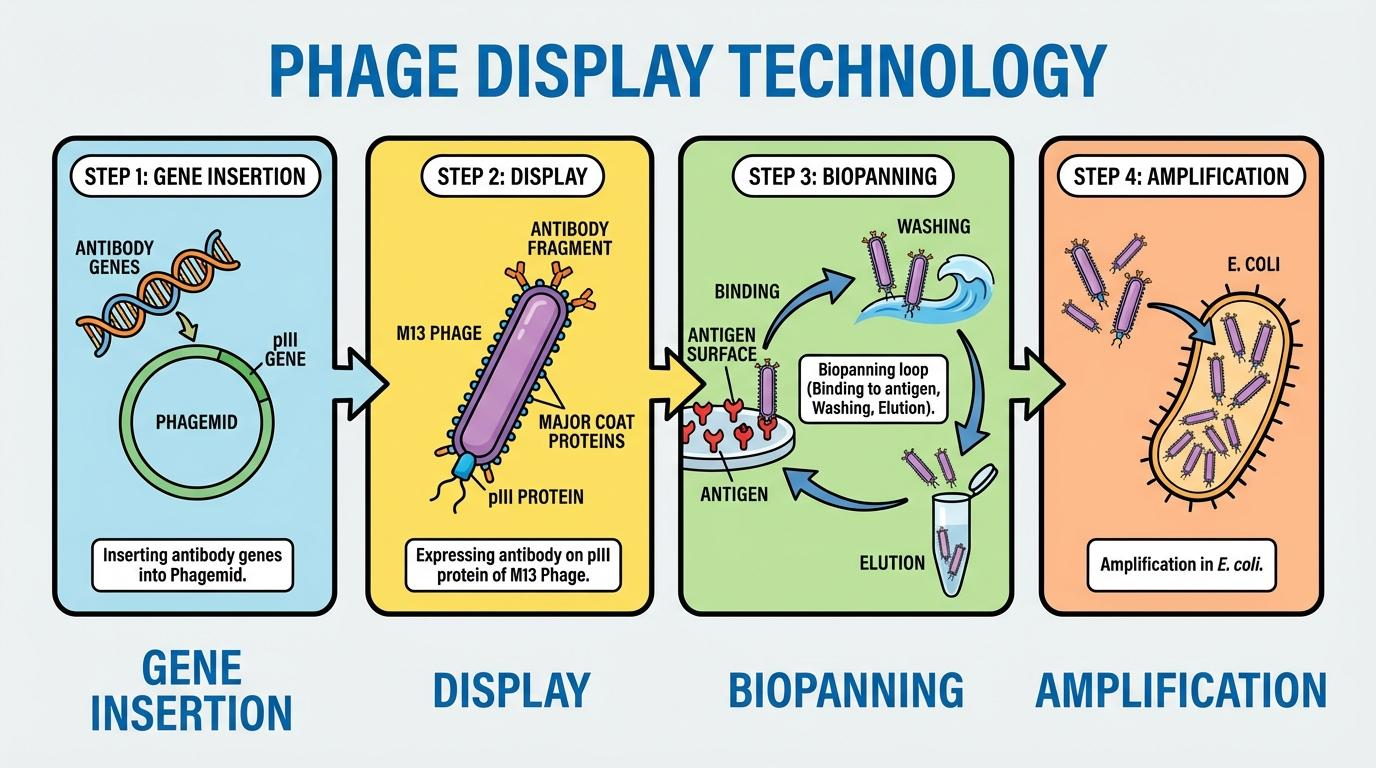
[그림 1] pIII 단백질을 통한 항체 표출 및 라이브러리 구축 단계
3. 항체 라이브러리 구축을 위한 파지미드와 헬퍼 파지의 협업 전략
효율적인 항체 스크리닝을 위해 연구자들은 파지미드(Phagemid) 시스템을 도입했습니다. 이는 항체 유전자를 담은 작은 벡터와, 파지의 조립에 필요한 모든 부속품을 제공하는 헬퍼 파지(Helper Phage)를 분리하여 운영하는 방식입니다.
| 시스템 구성 | 주요 기능 | 보유 유전자 |
|---|---|---|
| 파지미드 (Phagemid) | 항체 유전자 보존 및 발현 | scFv-pIII 융합 유전자, 선택 마커(Amp) |
| 헬퍼 파지 (Helper Phage) | 파지 입자 조립 및 복제 지원 | 모든 코트 단백질, 복제 효소 (M13KO7 등) |
4. 바이오팬닝 공정: 최적의 항체를 선별하는 4단계 메커니즘
구축된 항체 라이브러리에서 목적 항원을 인식하는 파지만을 골라내는 기술적 과정을 바이오팬닝 공정이라 부릅니다. 보통 3~5회차(Round)를 반복하며 선택 압력을 높여갑니다.
- Binding: 고정화된 항원에 파지 라이브러리를 반응시켜 결합을 유도합니다.
- Washing: Tween-20 등을 포함한 완충액으로 결합하지 않은 파지를 제거합니다. 회차가 거듭될수록 세척 횟수를 늘려 결합력이 낮은 파지를 탈락시킵니다.
- Elution: 낮은 pH나 특정 효소를 사용하여 항원에 붙은 파지만을 회수합니다.
- Amplification: 회수된 파지를 다시 대장균에 감염시켜 다음 라운드를 위한 충분한 양으로 증폭합니다.
이 공정의 핵심은 결합 속도(Ka)와 해리 속도(Kd)의 균형을 맞추는 것입니다. 최종적으로 평형 해리 상수인 KD 값이 낮은, 즉 결합 친화도가 매우 높은 항체 클론을 확보하는 것이 목표입니다.
자주 묻는 질문 (FAQ)
Q: M13KO7 헬퍼 파지의 역할은 무엇인가요?
A: 파지미드 시스템에서는 파지 조립에 필요한 코트 단백질 유전자가 부족합니다. M13KO7은 이러한 유전자들을 보충해주어, 항체가 표출된 파지 입자가 정상적으로 만들어지도록 돕는 생산 도구 역할을 합니다.
Q: 바이오팬닝 과정에서 왜 농축도(Enrichment)를 확인해야 하나요?
A: 각 라운드마다 회수된 파지의 양이 늘어난다는 것은 특정 항원에 결합하는 파지들이 선택적으로 증폭되고 있다는 지표이기 때문입니다.
핵심 용어 정리 (Glossary)
- scFv (Single-chain Variable Fragment): 항체의 VH와 VL 도메인을 유연한 펩타이드 링커로 연결한 단백질.
- pIII Protein: M13 파지의 감염과 유전자 주입을 담당하는 말단 코트 단백질.
- Affinity Maturation: 바이오팬닝을 통해 항체의 결합력을 인위적으로 높이는 과정.
- Ka / Kd: 항원-항체 결합 속도 상수 및 해리 속도 상수.
※ 본 콘텐츠의 상표명(M13, Humira 등)은 해당 소유권자의 자산이며, 정보 전달 목적으로만 사용되었습니다.
문의 QR 코드 (메시지 연결)