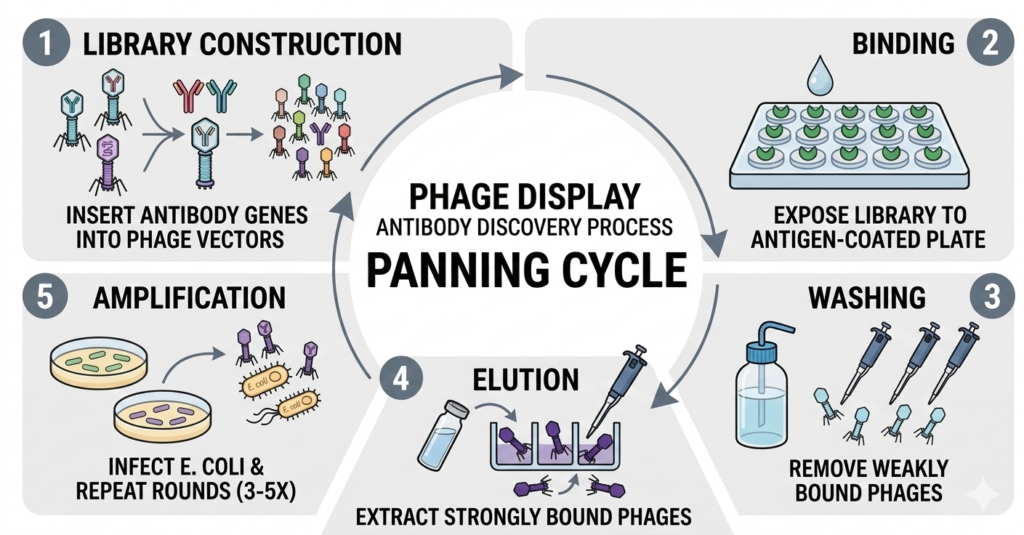
성공적인 항체 발굴 파이프라인 전략은 초기 단계에서 104개 이상의 후보군을 신속하게 거르고, 실제 세포 환경(In cellulo)에서의 생물학적 유효성을 조기에 검증하는 것에 있습니다. 단순히 결합력(Binding)만 보는 것이 아니라, ADC의 경우 내부화(Internalization) 효율을, 일반 항체의 경우 에피토프(Epitope)의 기능적 특이성을 우선순위에 두어야 임상 단계의 실패율을 낮출 수 있습니다.
바이오 벤처와 연구소의 항체 신약 파이프라인에서 발생하는 가장 큰 손실은 ‘잘 붙지만 작동하지 않는’ 후보물질에 과도한 리소스를 투입하는 것입니다. 수만 개의 라이브러리에서 단 하나의 최종 후보를 찾아가는 과정은 정밀한 스크리닝 파이프라인 설계가 뒷받침되어야 합니다.
항체 발굴 파이프라인 전략: 깔때기(Funnel)형 검증 설계
효율적인 후보물질 검증 흐름의 핵심은 속도와 정확도의 최적 배분입니다. 초기에는 정제 단백질을 이용한 대량 스크리닝을 진행하고, 후기에는 복잡한 세포 수준의 데이터를 확보하여 개발 가능성을 타진해야 합니다.
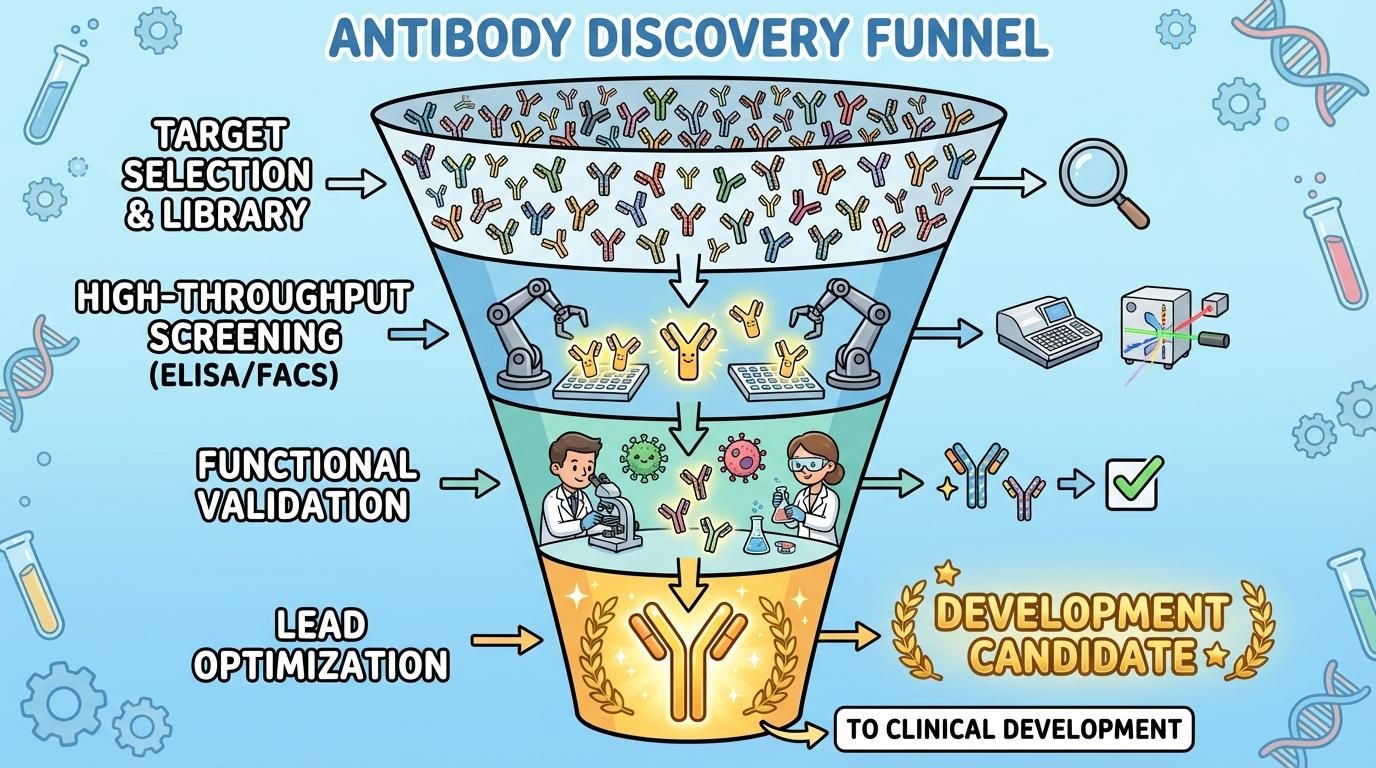
[그림 1] 항체 발굴의 단계별 필터링 구조: 수만 개의 클론이 단 하나의 후보가 되는 과정
1. 단계별 스크리닝 프로세스
- Step 01. 1차 High-throughput 스크리닝: ELISA, Bead-based assay 등을 통해 수만 개의 클론을 1~2일 내에 처리합니다. 이때는 위음성(False Negative)을 줄이기 위해 다소 완화된 컷오프를 적용합니다.
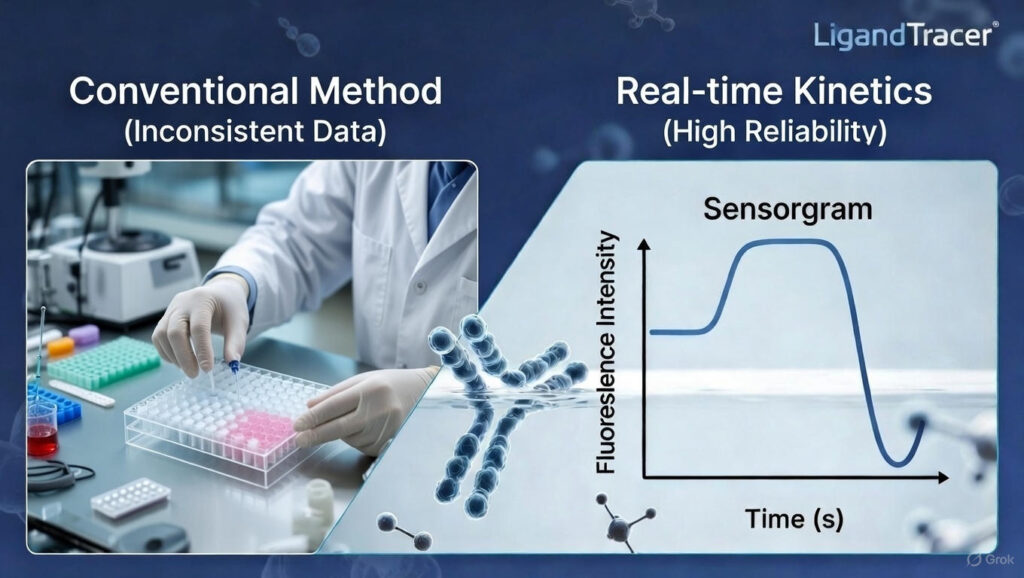
- Step 02. 2차 정밀 검증: SPR(표면 플라즈몬 공명)이나 BLI를 통해 결합 속도(ka)와 해리 속도(kd)를 분석합니다. 또한 종간 교차반응(Cross-reactivity)을 확인하여 전임상 모델 적용 가능성을 판단합니다.
- Step 03. 세포 결합 및 기능 검증: FACS(유세포 분석) 기반의 세포 결합 assay를 통해 실제 수용체 밀도와 환경에서의 효능을 검증합니다.
스크리닝 기술별 성능 및 효율 비교
| 분석 기술 | 처리량 (Throughput) | 데이터 정밀도 | 주요 산출값 |
|---|---|---|---|
| ELISA | 매우 높음 (10,000+) | 낮음 | Binding OD value |
| SPR (Biacore 등) | 보통 (100~300) | 매우 높음 | ka, kd, KD (Kinetics) |
| FACS (Cell binding) | 낮음 (50~100) | 보통 (실제 환경) | MFI, EC50 |
ADC 개발을 위한 항체 최적화 특이점
ADC(Antibody-Drug Conjugate)를 위한 항체 신약 파이프라인은 일반 치료용 항체와 설계 궤가 다릅니다. 단순히 ‘강하게 붙는’ 것보다 ‘세포 내부로 약물을 얼마나 효율적으로 운반하는가’가 핵심입니다.
- 결합 친화도(Affinity): 무조건 높은 친화도가 좋은 것은 아닙니다. 너무 강한 결합은 종양 내부 침투(Tumor Penetration)를 방해할 수 있으므로 1~10 nM 수준의 적절한 KD 값이 선호되기도 합니다.
- 내부화(Internalization) 속도: 약물 접합 후에도 항체가 세포 내 lysosome까지 도달하는 속도를 조기에 평가해야 합니다.
- 접합 안정성(Conjugation Stability): DAR(Drug-to-Antibody Ratio)이 높아져도 항체의 응집(Aggregation)이 발생하지 않는지 물리화학적 안정성을 먼저 체크하십시오.
면역원성 예측: 개발 후기 리스크 관리
항체 치료제의 가장 큰 복병은 임상에서 나타나는 ADA(Anti-Drug Antibody) 형성입니다. 항체 발굴 파이프라인 전략 수립 시, 인실리코(In silico) 예측 툴을 활용해 T세포 에피토프를 사전에 제거하는 ‘De-immunization’ 과정이 포함되어야 합니다.
핵심 용어 정리 (Glossary)
- Avidity (결합력):
- 개별 결합(Affinity)이 합쳐져 나타나는 전체적인 결합 강도. 세포 표면 결합에서 특히 중요합니다.
- Epitope (항원 결정기):
- 항체가 항원의 특정 부위에 결합하는 부위. 에피토프에 따라 기능성(Agonist vs Antagonist)이 결정됩니다.
- In silico Analysis:
- 컴퓨터 시뮬레이션을 통해 항체의 서열, 구조, 면역원성 등을 예측하는 기법.
자주 묻는 질문 (FAQ)
Q1: 1차 스크리닝에서 컷오프(Cut-off)는 보통 어느 정도로 잡나요?
A1: 정답은 없으나, 보통 상위 10~15% 수준의 OD 값을 가진 클론을 2차로 올립니다. 하지만 타깃의 특성에 따라(예: 막단백질) 조금 더 느슨하게 잡아 유효 후보의 유실을 방지하는 것이 전략적일 수 있습니다.
Q2: 면역원성 예측 툴 중 무료로 사용할 수 있는 것이 있나요?
A2: NetMHCpan과 같은 서버는 학술용으로 널리 쓰이지만, 기업용 파이프라인에서는 데이터 보안과 HLA 다양성 반영을 위해 EpiMatrix나 TAP 같은 상용 툴을 활용하는 것이 일반적입니다.
참고 문헌 및 출처
- YclueBio, “Antibody Internalization in ADC Development Guide”, 2024.
- Creative Biolabs, “Key Points of ADC Optimization Strategy”, 2024.
- E. Matrix et al., “In silico strategies for immunogenicity prediction”, Journal of Biotech, 2023.
※ 언급된 모든 제품명 및 서비스명은 해당 소유자의 등록 상표입니다.
자주 묻는 질문 (FAQ)
Q1: 1차 스크리닝에서 컷오프(Cut-off)는 보통 어느 정도로 잡나요?
A1: 정답은 없으나, 보통 상위 10~15% 수준의 OD 값을 가진 클론을 2차로 올립니다. 하지만 타깃의 특성에 따라(예: 막단백질) 조금 더 느슨하게 잡아 유효 후보의 유실을 방지하는 것이 전략적일 수 있습니다.
Q2: 면역원성 예측 툴 중 무료로 사용할 수 있는 것이 있나요?
A2: NetMHCpan과 같은 서버는 학술용으로 널리 쓰이지만, 기업용 파이프라인에서는 데이터 보안과 HLA 다양성 반영을 위해 EpiMatrix나 TAP 같은 상용 툴을 활용하는 것이 일반적입니다.
참고 문헌 및 출처
- YclueBio, “Antibody Internalization in ADC Development Guide”, 2024.
- Creative Biolabs, “Key Points of ADC Optimization Strategy”, 2024.
- E. Matrix et al., “In silico strategies for immunogenicity prediction”, Journal of Biotech, 2023.
※ 언급된 모든 제품명 및 서비스명은 해당 소유자의 등록 상표입니다.
문의 QR 코드 (메시지 연결)