항체-분해약물접합체(DAC)는 항체의 정밀 타격 능력과 TPD(Targeted Protein Degradation)의 촉매적 분해 성능을 결합하여 기존 ADC의 좁은 치료지수(TI) 문제를 획기적으로 해결하는 차세대 모달리티입니다. 이 기술은 유비퀴틴-프로테아좀 시스템을 활용해 질환 단백질을 근본적으로 제거하며, 항암제 내성 극복과 치료 효능 극대화(약 10-100배 낮은 용량으로도 효과 입증)를 가능하게 하는 혁신적인 해결방안을 제시합니다.
신약 개발 연구 현장에서 가장 큰 과제는 치료지수(Therapeutic Index, TI)의 확보입니다. 강력한 효능을 내면서도 정상 세포에는 독성을 끼치지 않는 적정 농도를 찾는 것은 생존과 직결된 문제입니다. 최근 항암제 시장의 중심인 ADC가 독성 문제로 난항을 겪는 가운데, 그 대안으로 떠오른 항체-분해약물접합체(DAC)에 대해 심도 있게 알아보겠습니다.
1. 항체-분해약물접합체(DAC)란 무엇인가?
항체-분해약물접합체(Degrader-Antibody Conjugate, DAC)는 기존 ADC에서 독성 화합물인 페이로드(Payload) 대신 표적 단백질 분해제(Degrader)를 항체에 결합한 형태입니다.
기존 Inhibitor 방식이 단백질의 활성 부위를 일시적으로 차단했다면, DAC는 세포 내 유비퀴틴-프로테아좀 경로를 활성화하여 질환의 원인이 되는 단백질을 아예 분해하여 사라지게 만듭니다. 이는 단백질 기능을 1:1로 억제하는 것을 넘어, 하나의 DAC 분자가 수십 개의 단백질을 연쇄적으로 파괴하는 ‘촉매적(Catalytic)’ 작용을 수행함을 의미합니다.
2. 기존 기술의 한계와 DAC의 등장 배경
DAC는 ADC의 오프-타겟 독성과 TPD의 낮은 생체 이용률이라는 고질적인 난제를 해결하기 위해 등장했습니다.
| 비교 항목 | ADC (기존) | TPD (PROTAC) | DAC (차세대) |
|---|---|---|---|
| 핵심 기전 | 세포 사멸 (직접 독성) | 촉매적 단백질 분해 | 표적 특이적 촉매 분해 |
| 특이성 | 높음 (항체 기반) | 낮음 (전신 노출) | 최상 (항체 정밀 유도) |
| 치료지수 (TI) | 제한적 (좁음) | 관리 필요 | 획기적 확장 가능 |
3. DAC의 정밀 작동 메커니즘
DAC가 세포 내에서 작용하는 과정은 4단계의 정교한 공정으로 이루어집니다.
단계 1: 항원 결합 및 내입(Internalization)
항체가 암세포 표면의 특이 항원을 인식하여 결합한 후, 엔도시토시스를 통해 세포 내부로 유입됩니다.
단계 2: 링커 절단 및 분해제 방출
세포 내 리소좀의 낮은 pH 환경이나 효소에 의해 링커가 끊어지며 분해제(Degrader)가 자유로운 상태가 됩니다.
단계 3: 삼중 복합체 형성
방출된 분해제는 질환 단백질과 세포 내 E3 리가아제(Ligase)를 물리적으로 연결하는 삼중 복합체를 형성합니다.
단계 4: 프로테아좀 분해 및 촉매 재생
유비퀴틴이 태그된 단백질은 프로테아좀에 의해 분해되며, 분해제는 다시 방출되어 다른 표적을 찾는 촉매 활동을 반복합니다.
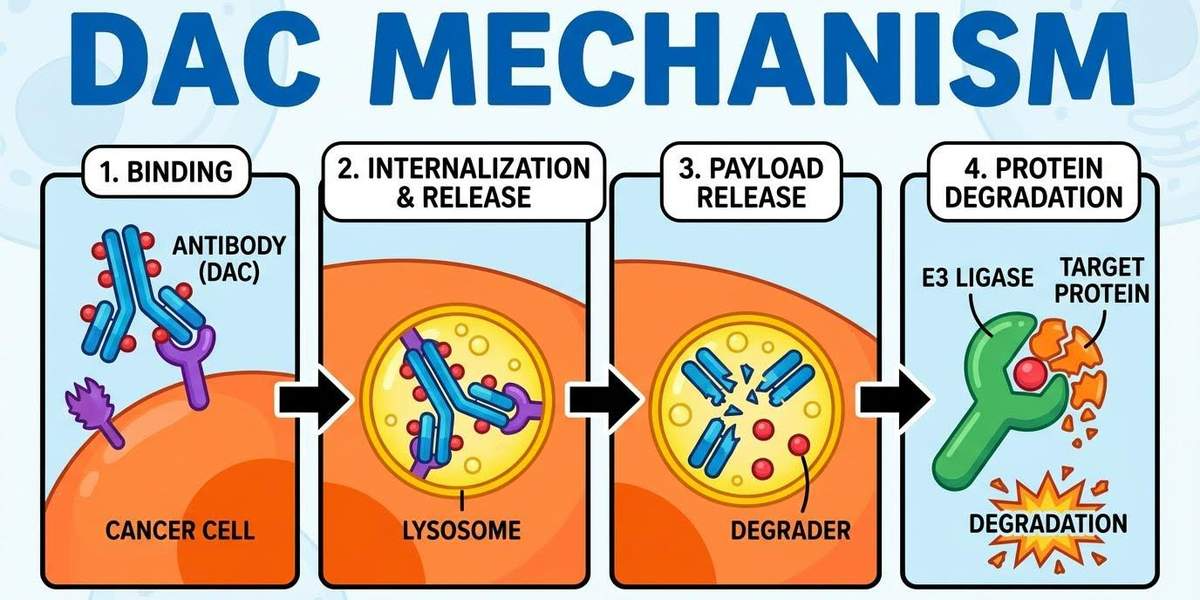
그림 1: 항체-분해약물접합체(DAC)의 세포 내 작용 기전
4. 자주 묻는 질문 (FAQ)
A: ADC는 페이로드 자체의 세포 독성에 의존하지만, DAC는 단백질을 선택적으로 제거하는 ‘촉매’ 역할을 합니다. 따라서 훨씬 적은 양의 약물로도 동일한 치료 효과를 낼 수 있어 정상 세포에 미치는 영향을 최소화합니다.
A: 기존의 소분자 억제제(Inhibitor)로 공략하기 어려웠던 ‘Undruggable’ 타겟, 특히 구조적으로 활성 부위가 명확하지 않거나 변이가 잦은 신호전달 단백질들이 주요 타겟입니다.
5. 핵심 용어 정리 (Glossary)
- 치료지수 (Therapeutic Index, TI): 약물의 유효 용량과 독성 유발 용량 사이의 비율. 이 값이 클수록 약물의 안전성이 높음을 의미합니다.
- E3 리가아제 (E3 Ligase): 표적 단백질에 유비퀴틴을 부착하여 분해 신호를 보내는 핵심 효소입니다.
- DAR (Drug-to-Antibody Ratio): 항체 한 분자당 결합된 약물(분해제)의 평균 개수로, DAC의 품질 관리 주요 지표입니다.
- SPR 분석: 표면 플라즈몬 공명 기술을 이용해 항체-항원 간의 결합 속도(ka)와 해리 속도(kd)를 실시간 측정하는 분석법입니다.
6. 참고문헌
- Maneiro, M. et al. (2024). “Degrader-Antibody Conjugates: The Next Frontier in Targeted Therapy.” *Nature Reviews Drug Discovery*.
- Genentech Research Report (2025). “Advancements in DAC Linker Technology for Oncology.”
- Korean Bio-Venture Association. “Analysis of Next-Gen Biopharmaceutical Modalities.”
정밀한 항체 분석과 신뢰도 높은 데이터가 필요하십니까?
와이클루바이오는 SPR, Binding Kinetics 분석부터 차세대 항체 발굴까지,
여러분의 DAC 프로젝트 성공을 위한 최고의 기술 파트너가 되어 드립니다.
본 포스팅에 언급된 상표권은 각 소유주에게 있으며, 본문은 정보 제공 목적으로만 작성되었습니다.
문의 QR 코드 (메시지 연결)