항체 개발 SPR 분석 및 항체 의약품 분석의 필수성
항체 의약품 개발에서 항체 개발 SPR 분석은 실시간 동역학(Kinetics) 데이터를 통해 항체-항원 결합의 정확한 ka, kd, KD 값을 라벨 없이 측정하는 유일한 표준 방법입니다. 이는 ELISA가 놓치기 쉬운 ‘Fast-off’ 항체를 선별하고, 생체 내 반감기(FcRn 결합)를 정확히 예측하여 신약 개발의 임상 실패 리스크를 획기적으로 낮춥니다.
핵심 키워드: #항체개발SPR분석 #Kinetics #반감기최적화 #식약처표준 #항체결합력측정
성공적인 신약 파이프라인 구축을 위해 항체 개발 SPR 분석은 이제 선택이 아닌 필수 공정으로 자리 잡았습니다. 글로벌 항체 의약품 시장이 급성장함에 따라, 단순히 ‘잘 결합하는가’를 넘어 ‘얼마나 빠르게 결합하고 얼마나 오래 유지되는가’에 대한 정밀한 데이터가 신약 승인의 성패를 가르기 때문입니다. 기존의 ELISA 방식만으로는 실제 임상 환경에서의 약효 지속 시간을 오판할 위험이 크기에, SPR을 통한 정밀한 동역학 분석이 연구 현장에서 강력히 요구되고 있습니다.
1. 항체 결합력 측정의 혁신: SPR의 실시간 동역학 우위
SPR(Surface Plasmon Resonance)은 종말점(End-point) 분석인 ELISA와 달리, 결합이 일어나는 전 과정을 실시간으로 모니터링합니다. 특히 항체 개발 SPR 분석을 활용하면 다음과 같은 결정적인 데이터 확보가 가능합니다.
- False Negative 방지: 결합력(Affinity)은 높지만 해리 속도(kd)가 빠른 항체는 세척 과정이 포함된 ELISA에서 누락되기 쉽습니다. SPR은 이를 실시간으로 포착하여 우수한 후보 물질의 유실을 막습니다.
- Avidity 분석: 항체의 이가(Bivalent) 구조에서 발생하는 다가 결합 세기를 정밀하게 분석해 실제 생체 내 효능을 더 정확하게 예측합니다.
- Label-free 분석: 형광 물질이나 효소를 부착하지 않아 단백질 본연의 네이티브 구조를 유지한 상태로 분석이 가능하며, 이는 데이터의 신뢰성을 높입니다.
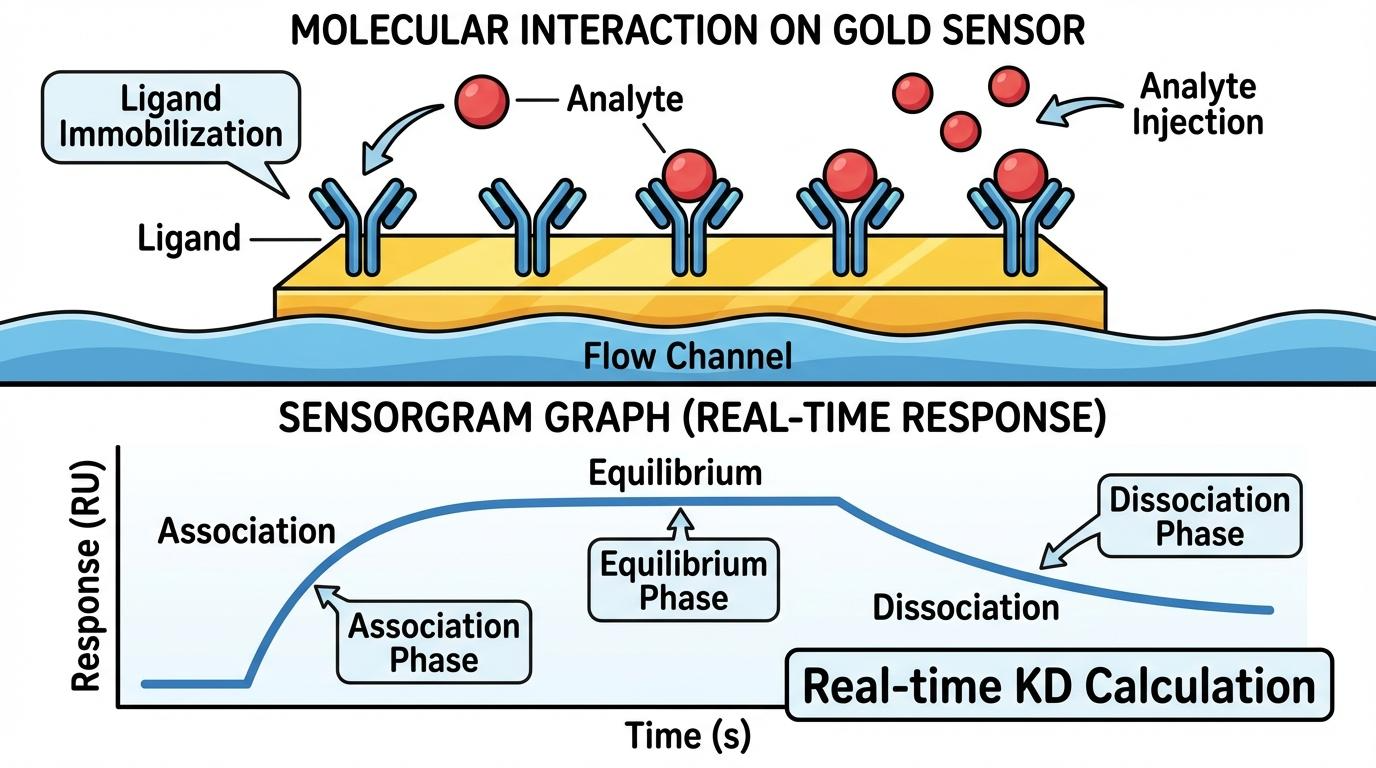
[그림 1] SPR 센서그램의 단계별 분석: Association(결합), Equilibrium(평형), Dissociation(해리)
2. SPR 신약 개발을 위한 전략적 선택: ELISA vs SPR 분석
연구 단계와 목적에 따라 적절한 분석법을 선택하는 것이 프로젝트의 효율성을 결정합니다.
| 비교 항목 | ELISA | SPR (Surface Plasmon Resonance) |
|---|---|---|
| 데이터 특성 | 정적 분석 (Affinity) | 동적 분석 (Kinetics: ka, kd) |
| 해리 과정 측정 | 불가능 | 실시간 가능 |
| 분석 속도/처리량 | 높음 (High Throughput) | 중간 (정밀 분석 위주) |
| 권장 활용 단계 | 초기 대량 후보물질 스크리닝 | 후보물질 검증, 임상 준비, QC |
바이오 벤처 팀장님들이라면 초기엔 비용 효율적인 ELISA로 Pool을 좁히고, 선별된 TOP 5 후보군에 대해서는 반드시 SPR 데이터를 확보하십시오. 특히 kd(해리 속도) 값이 약효 지속 시간과 직결되므로, KD 값만 보고 판단하는 우를 범하지 말아야 합니다.
3. 항체 의약품 분석의 핵심: FcRn 상호작용 및 반감기 최적화
항체 의약품의 가장 큰 경쟁력은 긴 반감기입니다. 일반적인 IgG 항체의 혈중 반감기는 약 21일에 달하는데, 이는 FcRn(Neonatal Fc Receptor)과의 pH 의존적 결합 메커니즘 때문입니다.
- pH 6.0 결합의 중요성: 산성 엔도솜 조건(pH 6.0)에서 FcRn과 강하게 결합하여 분해를 피하고 재순환되는지 여부를 SPR로 정밀 측정합니다.
- 엔지니어링 검증: YTE 변이 등 Fc 영역 엔지니어링을 통해 반감기를 늘릴 때, SPR은 pH 조건별(pH 6.0 vs pH 7.4) 결합 속도 변화를 수치화하여 최적의 디자인을 확증합니다.
4. 항체 개발 SPR 분석 규제 근거: 식약처 및 글로벌 표준
단순한 연구용 데이터를 넘어 상용화를 위해서는 규제 기관의 기준을 충족해야 합니다. 실제 실무 현장에서 항체 개발 SPR 분석 결과는 인허가 승인을 위한 결정적 근거로 활용됩니다.
- 식약처 지침: “항체의약품 품질평가 시험정보집”에서는 TNF-alpha 특이적 SPR 분석을 역가 시험의 표준 예시로 명시하고 있습니다.
- 글로벌 표준: EMA와 FDA 역시 FcRn Binding Assay를 PK/PD 데이터의 핵심 근거로 인정하며, Biacore 등의 SPR 장비 데이터를 표준으로 채택하고 있습니다.
- 승인 리스크 관리: IND/NDA 제출 시 SPR 데이터 누락은 보완 요구 및 심사 지연의 주요 원인이 됩니다.
핵심 용어 정리 (Glossary)
• ka (Association Rate Constant): 항체와 항원이 얼마나 빨리 결합하는지를 나타내는 속도 상수.
• kd (Dissociation Rate Constant): 결합된 항체와 항원이 얼마나 빨리 떨어지는지를 나타내는 상수. 약효 지속성(Duration)의 지표.
• KD (Equilibrium Dissociation Constant): 평형 해리상수. kd/ka로 계산되며, 값이 작을수록 결합 친화도(Affinity)가 강함을 의미.
• Sensorgram: SPR 장비에서 실시간으로 기록되는 결합 반응 곡선.
자주 묻는 질문 (FAQ)
Q1. ELISA 데이터만으로 IND(임상시험계획) 제출이 가능한가요?
A1. 가능은 하지만 리스크가 큽니다. 최근 식약처 및 글로벌 규제 기관은 항체의 결합 기전(MoA)을 설명하기 위해 상세한 Kinetics 데이터를 요구하는 추세입니다. 특히 바이오시밀러 개발 시 SPR 데이터는 필수입니다.
Q2. SPR 분석 시 가장 주의해야 할 수치는 무엇인가요?
A2. 많은 연구자들이 KD(친화도)에만 집중하지만, 실제 생체 내 효능은 kd(해리 속도)에 의해 좌우되는 경우가 많습니다. ‘얼마나 오래 붙어있는가’가 약효를 결정하기 때문입니다.
참고문헌 및 근거 자료
- 식품의약품안전처, 항체의약품 품질평가 시험정보집 (2017)
- EMA/FDA ICH Q6B 가이드라인: Specification for Biotechnological Products
- YclueBio Technical Note: SPR vs ELISA Affinity Analysis Guide
- Journal of Antibodies: FcRn-IgG Interaction and Half-life Optimization (2016)
본 포스팅은 항체 개발 연구를 돕기 위한 정보 제공 목적으로 작성되었습니다. ‘Biacore’는 Cytiva의 등록 상표입니다.
문의 QR 코드 (메시지 연결)