신약 개발에서 Binding Affinity 차이가 발생하는 근본적인 원인은 리셉터의 존재 환경에 있습니다. 재조합단백질은 정제된 상태로 일관된 데이터를 제공하지만, 실제 세포표면 리셉터는 PTM(당쇄화), Dimerization, 그리고 세포 내 구획의 동적인 변화에 따라 결합력(KD)이 최대 10배 이상 달라질 수 있습니다. 정확한 약물 효능 예측을 위해서는 SPR 분석 서비스와 함께 LigandTracer를 활용한 실시간 ka, kd 측정 및 1:2 Heterogeneous 모델 분석이 병행되어야 합니다.
핵심 키워드: #BindingAffinity차이 #세포표면리셉터 #재조합단백질 #BindingKinetics #KD분석
Binding Affinity 차이가 발생하는 근본적인 이유는 무엇일까요?
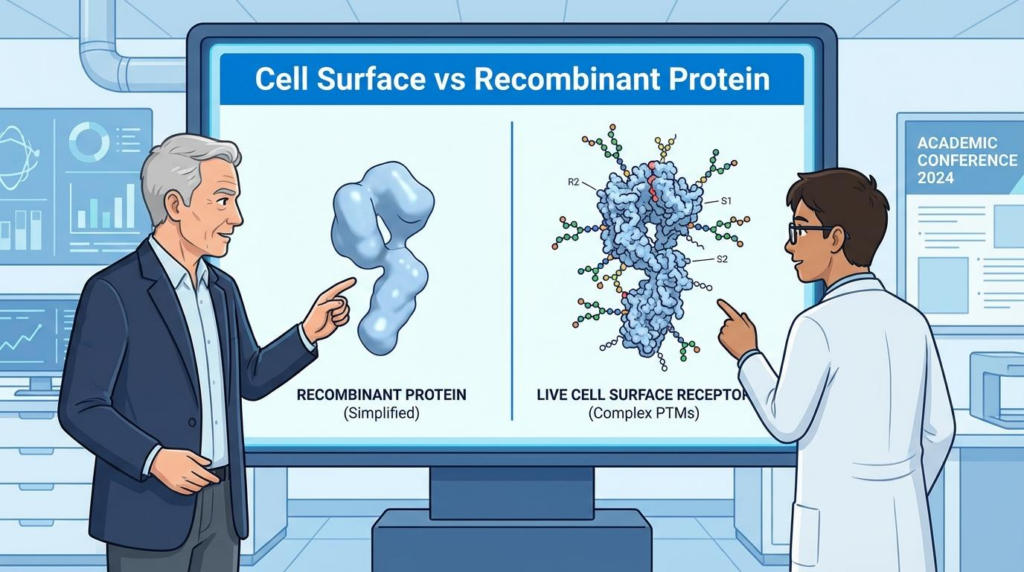
신약 후보 물질을 발굴하는 초기 단계에서 연구원들은 재조합단백질을 이용한 스크리닝에 의존합니다. 하지만 이 과정에서 얻은 Binding Affinity(KD) 수치가 실제 세포 수준의 실험이나 임상 단계에서 재현되지 않는 경우가 빈번합니다. 이는 정제된 단백질과 살아있는 세포표면 리셉터 사이의 구조적, 환경적 괴리에서 기인합니다.
구체적인 데이터로 살펴보면, Björkelund et al. (2011)의 연구에서는 A431 암세포 표면의 EGFR과 재조합 EGFR 단백질에 대한 EGF의 결합력을 비교했습니다. 결과적으로 세포표면 리셉터는 재조합단백질 대비 약 10배에서 15배 더 강한 avidity를 나타냈으며, 이는 단순히 수치상의 차이를 넘어 약물의 유효 농도 결정에 치명적인 영향을 미칠 수 있음을 시사합니다.
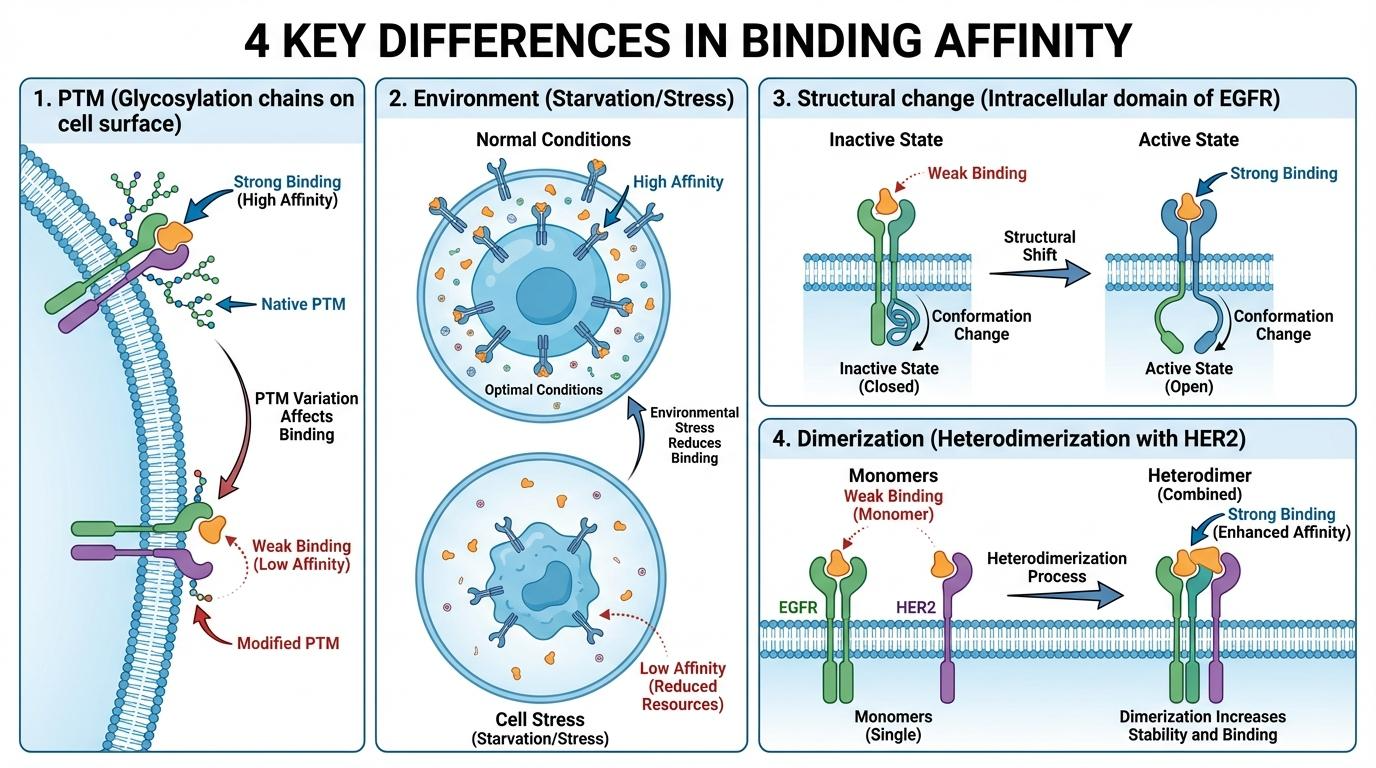
[그림 1] Binding Affinity 차이를 유발하는 세포막 환경의 복잡성 비교
Binding Kinetics 측정 시 세포표면 리셉터와 재조합단백질은 어떤 차이가 있을까요?
1. PTM(Post-Translational Modification)과 Glycosylation의 영향
재조합단백질은 대량 생산 과정에서 암세포 특유의 Glycosylation(당쇄화) 패턴을 그대로 복제하지 못합니다. 예를 들어, 종양 세포 표면에서는 특정 당쇄화 패턴이 20% 이상 증가하여 리셉터의 Natural Conformation을 유지시키는 반면, 정제된 단백질은 이러한 PTM이 결여되어 ka(결합 속도)가 실제보다 느리게 측정되거나 결합 부위가 노출되지 않을 수 있습니다.
2. Gefitinib 기전으로 본 Intracellular 도메인의 역할
비소세포폐암 치료제인 Gefitinib은 EGFR의 세포 내 Tyrosine Kinase 부위에 결합합니다. 이 약물이 결합하면 리셉터 전체의 구조적 전이가 발생하여 외부 도메인의 Binding Kinetics를 변화시킵니다. 하지만 대다수의 재조합단백질 분석은 ECD(Extracellular Domain)만을 사용하므로, 이러한 약물에 의한 2차적 Affinity 변화를 관찰하는 것이 불가능합니다.
약물 스크리닝 시 SPR 분석 서비스로 일차적인 ka, kd 측정을 마쳤다면, 상위 5% 후보 물질에 대해서는 반드시 세포표면 리셉터 기반의 실시간 결합 분석을 수행해야 합니다. 특히 HER2와 EGFR이 공존하는 SKOV3 세포주와 같은 환경에서는 Dimerization에 의한 Heterogeneous Binding 양상이 30% 이상의 KD 값 편차를 유발할 수 있습니다.
3. 미세환경 스트레스와 결합 부위의 동적 변화
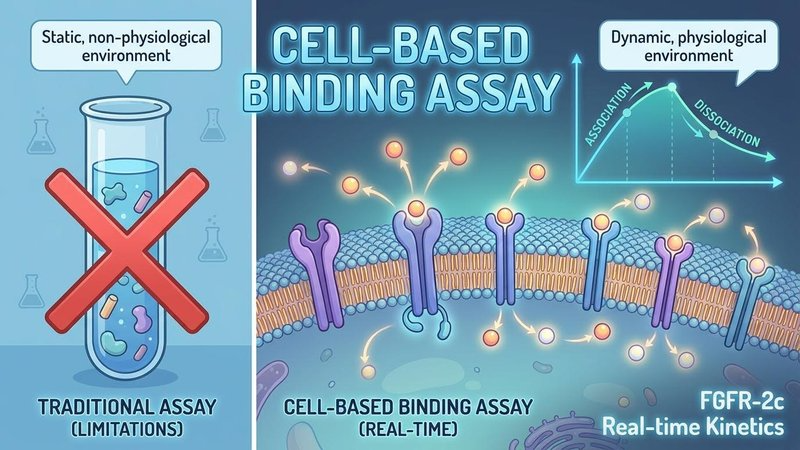
암세포는 Hypoxia(저산소) 및 Starvation(영양 부족) 스트레스에 직면할 때 생존을 위해 리셉터의 클러스터링을 유도하거나 내보냅니다. 이러한 동적인 Binding Affinity 차이는 정적 환경인 재조합단백질 실험에서는 절대로 재현될 수 없는 현상입니다. 살아있는 세포를 사용한 LigandTracer 분석만이 이러한 환경적 변수를 데이터에 반영할 수 있습니다.
정확한 KD 분석을 위한 기술별 특성 비교
분석의 목적에 따라 재조합단백질과 세포표면 리셉터 분석을 적절히 배분하는 전략이 필요합니다. 아래 표는 두 방식의 핵심 차이점을 요약한 것입니다.
| 분류 항목 | 재조합단백질 기반 (SPR/ELISA) | 세포표면 기반 (LigandTracer) |
|---|---|---|
| 데이터 특성 | 균일한 구조, 높은 재현성 | Heterogeneous, 실제 생체 모사 |
| Kinetics 모델 | 1:1 Langmuir 모델 적용 | 1:1 및 1:2 혼합 모델 적용 |
| 측정 파라미터 | 순수 결합 상수 (ka, kd) | Avidity, 내포화(Internalization) 포함 |
| 주요 한계점 | 세포막 및 PTM 영향 배제 | 분석 시간이 상대적으로 길어짐 |
자주 묻는 질문 (FAQ)
Q1. Binding Affinity 차이가 크게 나면 실험 데이터로서 가치가 없나요?
A. 가치가 없는 것이 아니라 데이터의 성격이 다른 것입니다. 재조합단백질은 분자 간의 ‘순수 결합력’을 보는 것이고, 세포표면 리셉터 분석은 복잡한 생체 환경에서의 ‘실질적 효능’을 예측하는 지표로 활용됩니다. 두 데이터를 교차 검증하는 것이 필수적입니다.
Q2. KD 분석 시 1:2 모델을 사용해야 하는 이유는 무엇인가요?
A. 세포 표면에는 결합 에너지가 다른 두 종류 이상의 결합 부위(예: High-affinity 및 Low-affinity site)가 동시에 존재할 수 있습니다. 1:1 모델로 강제 피팅할 경우 평균값이 왜곡되므로, ka1, ka2와 같이 분리된 상수를 얻기 위해 1:2 모델이 권장됩니다.
핵심 용어 정리 (Glossary)
- Binding Affinity 차이: 동일 타겟임에도 측정 환경(정제 단백질 vs 라이브 셀)에 따라 KD 값이 변하는 현상.
- ka (Association Rate): 단위 시간당 결합되는 분자 수. 약물의 ‘반응 속도’를 결정함.
- kd (Dissociation Rate): 결합된 상태를 유지하는 능력. 약물의 ‘지속성’과 직결됨.
- Dimerization: 두 개의 리셉터가 결합하여 복합체를 이루는 과정. 결합 친화도를 급격히 변화시키는 주요 요인.
- LigandTracer: 회전형 디쉬 원리를 이용하여 세포 표면의 결합 kinetics를 실시간으로 모니터링하는 전문 장비.
정교한 Binding Kinetics 데이터로 약물 가치를 높이세요
재조합단백질부터 실시간 세포 기반 분석까지 통합 솔루션을 제공합니다.
전문가 상담 신청하기문의 QR 코드 (메시지 연결)
본 포스트의 내용은 바이오 의약품 연구 개발의 일반적인 지침을 따르며, 특정 약물의 효능은 실험 조건에 따라 다를 수 있습니다.