Phage Display 항체 제작 과정: M13 박테리오파지의 원리부터 라이브러리 구축까지
오늘은 M13 박테리오파지의 독특한 생물학적 특성을 활용한 Phage Display 항체 제작 과정과 그 속에 숨겨진 과학적 원리를 심층적으로 알아보겠습니다.
1. 박테리오파지, 바이러스에서 항체 공장이 되기까지
박테리오파지는 박테리아를 감염시키는 바이러스로, 단백질 외피(캡시드) 안에 유전물질(DNA/RNA)을 담고 있는 단순한 구조를 가집니다. 일반적으로 파지는 숙주 세포 내에서 증식한 뒤 세포를 파괴(Lysis)하며 밖으로 나오지만, 항체 제작에 주로 쓰이는 M13 박테리오파지는 매우 독특한 생활사를 가집니다.
M13 박테리오파지의 독보적인 특징
비용해성(Non-lytic) 증식: 숙주 세포인 대장균(E. coli)을 죽이지 않고 세포막을 통해 지속적으로 바이러스 입자를 방출합니다. 이는 연속적인 단백질 생산과 대량 증식을 가능하게 하는 Phage Display의 최대 장점입니다.
단일 가닥 DNA(ssDNA): 조작이 용이한 유전 구조를 가지고 있어 외부 유전자를 삽입하기에 적합합니다
2. Phage Display 항체 제작 과정의 핵심: pIII 단백질
위치와 기능: pIII는 파지 입자의 한쪽 끝에 위치하며, 대장균에 부착하여 유전물질을 주입하는 통로 역할을 합니다.
항체와의 연결: 연구자들은 항체의 가변 부위인 Fab나 scFv 유전자를 이 pIII 유전자와 연결합니다.
표면 표출: 파지가 조립될 때, 삽입된 유전자에 의해 만들어진 항체가 pIII 단백질과 함께 파지 표면에 대롱대롱 매달린 형태로 나타나게 됩니다.
이론적으로 M13 파지는 5개의 pIII 단백질을 가지지만, 패키징 효율과 안정성을 위해 실제로는 파지당 1~3개의 항체가 결합된 형태로 제작됩니다.
3. Two Phage System: 효율을 극대화하는 전략
실제 연구 현장에서는 실험의 유연성과 대량 생산을 위해 Two Phage System을 주로 사용합니다. 이는 ‘파지미드(Phagemid)’와 ‘헬퍼 파지(Helper Phage)’의 협업 시스템입니다.
Phagemid-containing Phage (설계도 담당)
우리가 찾고자 하는 특정 항체 유전자를 담고 있습니다. 하지만 파지미드 스스로는 파지 입자를 완성할 모든 정보를 가지고 있지 않습니다.
Helper Phage (생산 도구 담당)
항체 유전자는 없지만, 파지의 복제와 패키징에 필요한 모든 효소와 코트 단백질을 제공합니다. 특히 Helper phage의 pIII는 항체가 달려있지 않아 파지 조립 과정을 방해하지 않고 효율적으로 인공 파지를 만들어냅니다.
[결과] Helper phage의 도움으로 대장균은 우리가 원하는 항체를 표면에 단 파지(Phagemid-containing phage)를 대량으로 복제해냅니다.
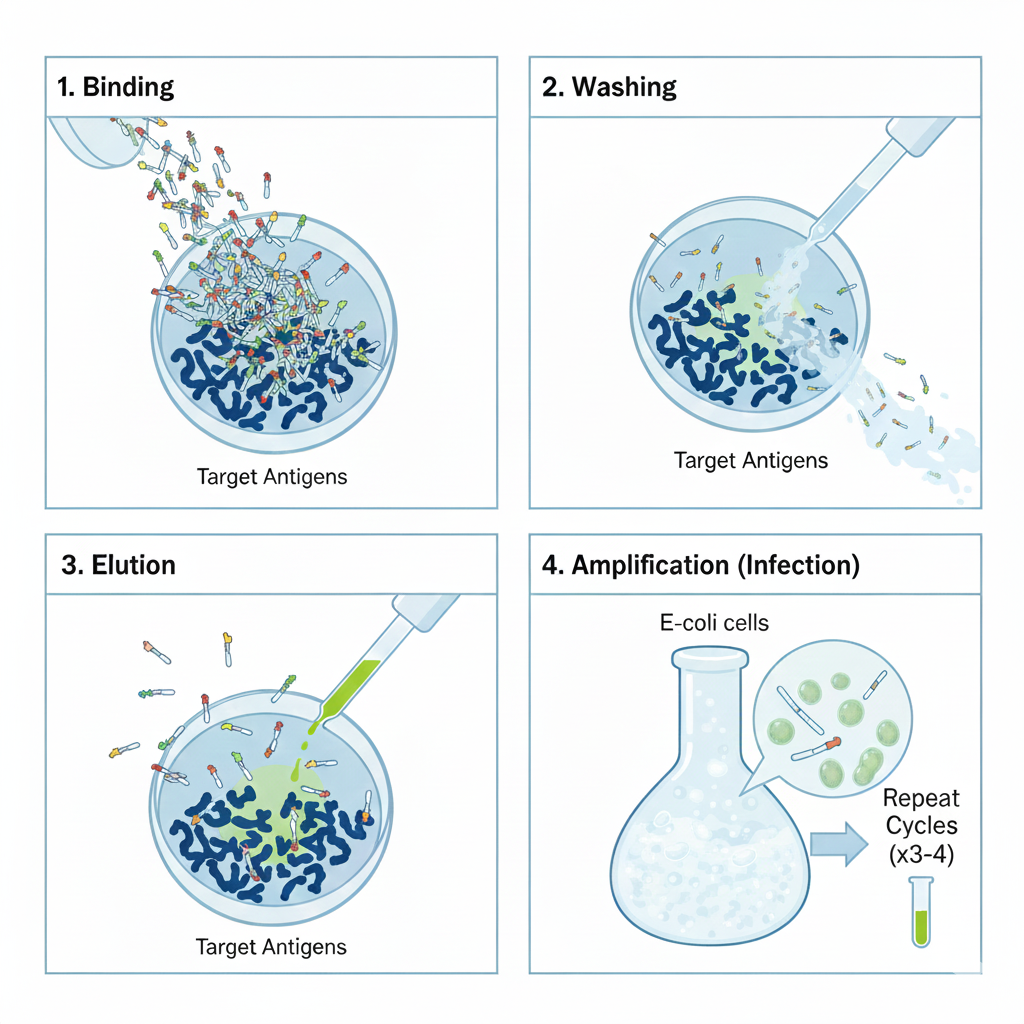
4. 항체 라이브러리 구축 및 스크리닝 (Biopanning)
결합(Binding): 항원이 코팅된 플레이트에 파지 라이브러리를 뿌립니다.
세척(Washing): 결합하지 못한 파지들을 씻어냅니다.
용출(Elution): 항원에 강하게 붙은 파지만을 떼어냅니다.
증폭(Amplification): 떼어낸 파지를 대장균에 다시 감염시켜 개체 수를 늘립니다.
이 과정을 3~4회 반복하면 특정 항원에 대해 결합력이 매우 높은 최적의 항체만을 선별할 수 있습니다.
5. 자주 묻는 질문 (Q&A)
Q: 왜 굳이 M13 파지를 사용하나요? A: 숙주 세포인 대장균을 파괴하지 않기 때문에 실험 관리가 용이하고, 바이러스 입자를 연속적으로 대량 얻을 수 있어 항체 스크리닝 효율이 압도적으로 높기 때문입니다.
Q: pIII 외에 다른 단백질은 사용 안 하나요? A: pVIII(p8) 단백질을 사용하기도 합니다. pVIII는 파지의 몸체를 구성하는 단백질로 수가 매우 많아(약 2,700개), 단백질을 훨씬 더 많이 표출하고 싶을 때 사용하지만 구조적 제약이 따릅니다.
6. 결론: 치료제 개발의 문을 여는 기술
Phage Display 항체 제작 과정은 단순한 생물학적 기작을 넘어, 현대 바이오 의약품의 초석이 되는 기술입니다. 특히 신속한 식별과 대량 증폭이라는 장점 덕분에 암, 자가면역질환 등 다양한 난치병 치료제 개발에 기여하고 있습니다.
정교하게 설계된 항체 라이브러리와 M13 파지의 복제 능력이 결합될 때, 우리는 비로소 질병을 정복하는 ‘마법의 탄환’에 한 걸음 더 다가갈 수 있습니다.