핵심 요약 (Summary)
단백질 상호작용 SPR 분석은 항체 개발 및 신약 스크리닝 과정에서 분자 간의 결합 동역학을 실시간으로 정량화하는 무표지(Label-free) 표준 기술입니다. 이 기술은 금 표면의 굴절률 변화를 감지하여 10-6에서 10-12 M 범위의 정밀한 평형 해리 상수(KD)를 산출하며, 단백질 결합 측정의 정확도를 극대화하여 후보 물질의 임상 성공 가능성을 예측하는 데 결정적인 역할을 합니다.
주요 키워드: PPI SPR 분석, 단백질 결합 측정, protein interaction, Biacore 시스템, 결합 동역학
단백질 상호작용 SPR 연구의 기술적 가치와 PPI 분석 필요성
현대 바이오 의약품 연구 환경에서 단백질 상호작용 SPR은 단순한 결합 여부 확인을 넘어, 결합의 ‘질적’ 특성을 규명하는 필수 도구입니다. 기존 ELISA가 제공하지 못하는 실시간 결합(Association) 및 해리(Dissociation) 데이터를 통해 protein interaction의 전 과정을 시각화함으로써, 연구원들은 더 정교한 약물 설계를 진행할 수 있습니다.
PPI SPR 분석 원리: 동역학적 데이터 도출 과정
SPR 센서 칩은 금속 표면의 전자 집단 진동 현상을 활용합니다. 리간드가 고정된 표면에 분석물(Analyte)이 흐르며 결합할 때 발생하는 질량 변화는 즉각적인 RU(Response Unit) 신호로 변환됩니다. PPI SPR 분석의 핵심 지표는 다음과 같습니다.
- ka (Association rate): 분석물이 리간드에 결합하는 속도 (M-1s-1). 약물의 타겟 인식 효율을 나타냅니다.
- kd (Dissociation rate): 결합된 복합체가 떨어져 나가는 속도 (s-1). 결합의 안정성을 의미합니다.
- KD (Affinity): kd를 ka로 나눈 값으로, 이 수치가 낮을수록 결합력이 강력함을 시사합니다.
정밀한 단백질 결합 측정을 위한 실험 설계 및 수치 데이터
성공적인 단백질 결합 측정을 위해서는 리간드 고정화(Immobilization) 전략이 중요합니다. 연구 현장에서는 주로 CM5 칩을 사용하며, 고정화 수준을 적절히 조절하여 대량 수송 제한(Mass transport limitation) 현상을 방지해야 합니다.
| 분석 단계 | 핵심 작업 내용 | 실무 수치 및 품질 기준 |
|---|---|---|
| 리간드 고정화 | EDC/NHS 화학 결합을 통한 표면 고정 | Kinetics 분석 시 100 ~ 500 RU 권장 |
| 분석물 주입 | 5단계 이상의 다농도 시리즈 테스트 | 농도 범위: 예상 KD 값의 0.1배 ~ 10배 |
| 데이터 모델링 | 1:1 Langmuir Global Fitting 적용 | Chi2 값이 Rmax의 10% 미만일 것 |
| 칩 재생 | 결합 물질 제거 및 표면 복원 | Regeneration 후 Baseline 편차 < 5 RU |
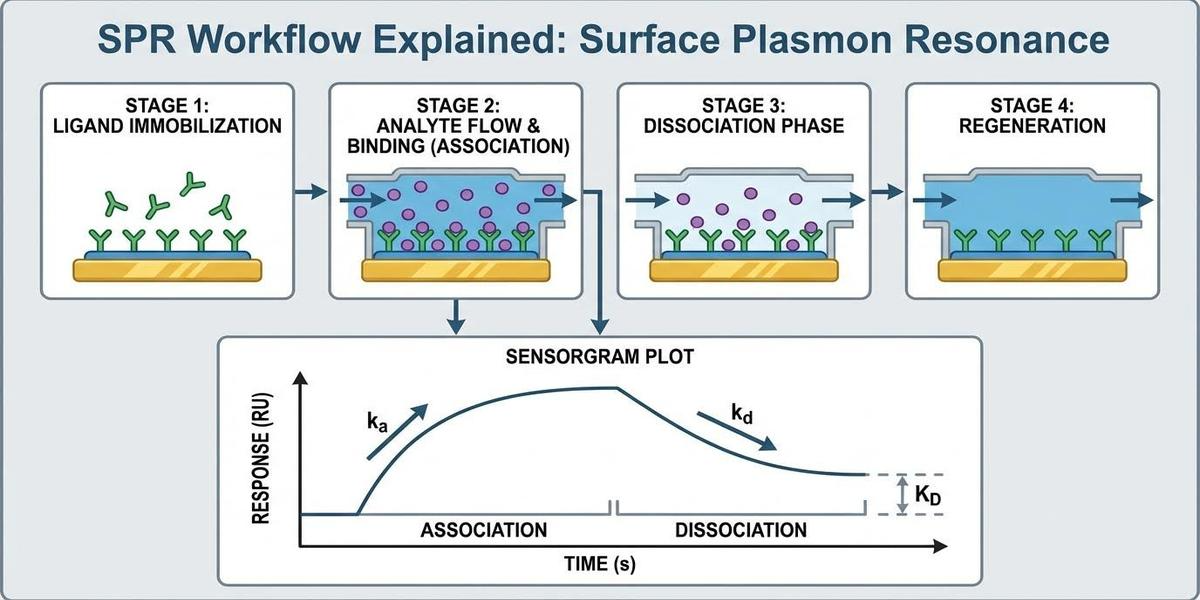
[그림 1] PPI SPR 분석의 전체 워크플로우와 동역학 파라미터 시각화 인포그래픽
글로벌 규제 기관의 단백질 상호작용 SPR 요구 조건
미국 FDA와 유럽약전(EP)은 바이오 의약품의 허가 과정에서 SPR 데이터를 강력하게 권고합니다. 특히 protein interaction의 정밀 데이터는 약물의 생물학적 유사성(Biosimilarity)을 입증하는 핵심 지표로 활용됩니다.
연구 실무자를 위한 규제 가이드라인
- FDA IND/BLA: 결합 속도(ka)와 해리 속도(kd)를 포함한 상세 Affinity Profile 제출.
- 유럽약전 (EP 10.0): EPO(에리스로포이에틴) 품질 평가 시 동물 실험 대신 SPR Assay를 표준으로 채택.
- 데이터 재현성: 독립적인 3회 이상의 반복 실험을 통해 CV(변동계수) 10% 이내 유지 필수.
연구 실무자를 위한 핵심 팁: 비특이적 결합 제어
단백질 상호작용 SPR 실험 시 데이터 노이즈의 주원인은 비특이적 결합입니다. 이를 해결하기 위해 러닝 버퍼에 CM-Dextran이나 0.05% Tween-20을 첨가하고, 주입 전 샘플을 버퍼와 동일한 조건으로 투석(Dialysis)하는 것이 데이터 신뢰도를 높이는 비결입니다.
분석 기법 비교: 왜 SPR이 표준인가?
PPI SPR 분석은 다른 분자 간 상호작용 분석 도구들과 비교했을 때 확실한 강점을 가집니다.
- vs ELISA: 평형 상태의 결과만 보는 ELISA와 달리, 결합이 일어나는 ‘과정’을 시간 단위로 분석 가능.
- vs ITC: 샘플 소모량이 매우 적고(µg 단위), 분석 속도가 5~10배 이상 빠름.
- vs Plate Reader: 단순 농도 의존적 결합 확인을 넘어, 약물이 타겟에 머무르는 시간(Residence time) 측정 가능.
핵심 용어 정리 (Glossary)
- Sensorgram (센서그램): 시간 흐름에 따른 신호 강도(RU) 변화를 나타낸 실시간 데이터 그래프.
- Bulk Effect (벌크 효과): 샘플과 버퍼의 굴절률 차이로 인해 결합과 상관없이 발생하는 일시적인 신호 점프.
- Rmax: 센서 표면의 모든 리간드가 분석물과 결합했을 때 나타나는 이론적 최대 반응값.
- Double Referencing: 레퍼런스 채널 신호와 버퍼 주입 신호를 모두 차감하여 순수 결합 신호만 추출하는 고도의 보정법.
자주 묻는 질문 (FAQ)
Q1. 단백질의 등전점(pI)이 고정화에 영향을 주나요?
A1. 네, 매우 중요합니다. 아민 커플링(Amine coupling) 시 단백질이 칩 표면으로 끌려가도록 하기 위해 단백질의 pI보다 낮은 pH의 버퍼(Pre-concentration buffer)를 선택해야 합니다.
Q2. SPR 장비 종류에 따라 데이터 차이가 큰가요?
A2. 기본 원리는 동일하지만 감도(Sensitivity)와 처리량(Throughput)에서 차이가 납니다. Biacore 8K와 같은 최신 장비는 이중 항체와 같은 복잡한 분자 분석에 더 유리합니다.
Q3. KD 값이 낮을수록 항상 좋은 약물인가요?
A3. 일반적으로는 그렇습니다. 하지만 실제 효능은 해리 속도(kd)에 의해 결정되는 ‘결합 유지 시간’에 더 큰 영향을 받는 경우가 많으므로 동역학 파라미터를 통합적으로 해석해야 합니다.
참고문헌
- Biacore Handbook: A Guide to Real-Time Molecular Interaction Analysis.
- FDA Guidance for Industry: Bioanalytical Method Validation (Binding Affinity focus).
- European Pharmacopoeia (Ph. Eur.) 10.0, Quality Control of Biological Products.
- Nature Methods: Trends in Label-free Protein-Protein Interaction Analysis.
상표권 고지: Biacore™ 및 CM5 칩은 Cytiva 그룹의 등록 상표입니다. 본 가이드는 연구용 정보 제공을 목적으로 하며, 특정 브랜드의 공식 매뉴얼과는 독립적으로 작성되었습니다.