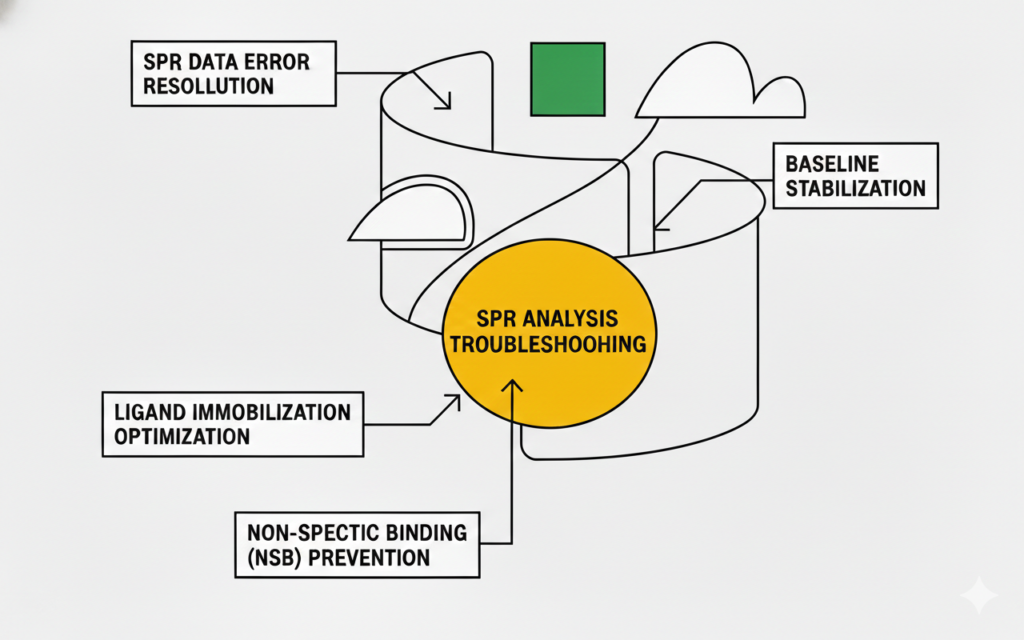
Surface Plasmon Resonance(SPR)는 라벨 없이 실시간으로 분자 간의 결합력을 측정할 수 있는 강력한 도구입니다. 하지만 바이오 연구 현장에서는 불안정한 베이스라인, 재현성 없는 데이터, 혹은 해석 불가능한 센서그램(Sensorgram)으로 인해 소중한 시약과 시간을 낭비하는 경우가 많습니다. 본 포스팅에서는 벤처 연구원 및 팀장님들이 실무에서 겪는 SPR 분석 트러블슈팅의 핵심 원인을 진단하고 즉각적인 해결 방안을 제시합니다.
💡 핵심 요약
SPR 데이터 오류의 약 70%는 버퍼 매칭 실패(RI Mismatch)와 버퍼 내 기포(공기) 제거 부족에서 기인합니다. 이를 해결하기 위해 샘플과 러닝 버퍼의 성분(pH, 염 농도, 첨가제 등)을 오차 없이 동일하게 맞추고, 유로 내에 기포가 생기지 않도록 기포를 충분히 제거한(Degassing) 버퍼와 고감도 센서칩(예: HC1000)을 사용해야 SPR 분석 트러블슈팅을 성공적으로 마칠 수 있습니다.
SPR 분석 트러블슈팅: 왜 데이터가 흔들리는가?
SPR 장비는 0.1 RU(Response Unit) 수준의 미세한 굴절률 변화를 감지합니다. 이는 장점이자 치명적인 단점이 되기도 합니다. 온도의 0.1°C 변화나 버퍼 내 DMSO 농도의 0.01% 차이만으로도 결과값은 크게 왜곡될 수 있습니다 (Myszka, 1999). 연구원이 마주하는 가장 흔한 문제는 다음과 같습니다.
🔍 알아두기: Drift(드리프트)란 무엇인가요?
쉽게 말해 ‘저울의 영점이 제멋대로 변하는 현상’입니다. 아무것도 올리지 않은 저울의 숫자가 0에서 1, 2, 3으로 계속 올라가거나 내려간다면 물건의 무게를 정확히 잴 수 없겠죠? SPR에서도 리간드와 분석물이 결합하지 않는 상태(평형 상태)에서는 신호가 수평을 유지해야 하는데, 이 기준선이 위나 아래로 기울어지는 것을 Drift라고 합니다.
- Baseline Drift: 칩 장착 직후 평형화 부족 혹은 리간드가 칩에서 미세하게 떨어져 나갈 때 발생합니다.
- Bulk Shift: 샘플과 러닝 버퍼 간의 굴절률 차이로 인해 그래프가 수직으로 툭 튀어 오르는 현상입니다.
- Non-Specific Binding (NSB): 분석물(Analyte)이 리간드가 아닌 칩 표면에 직접 들러붙는 현상입니다.
주요 에러 유형별 원인 및 즉각 조치 사항
실무 현장에서 가장 빈번하게 발생하는 4가지 에러 그룹을 체계적으로 분류하였습니다.
| 현상 (Error Type) | 주요 원인 | 해결 전략 (Troubleshooting) |
|---|---|---|
| Baseline Drift | 칩 평형화 부족, 리간드 해리 | Buffer Flow 20분 이상 유지, 리간드 공유 결합 강도 확인 |
| Bulk Shift (Spikes) | 버퍼 간 굴절률 차이, 기포 발생 | In-line Degasser(기포 제거 장치) 확인, 조성(DMSO 등) 정밀 일치 |
| Low Immobilization | pH Scouting 실패, 활성화 부족 | Ligand pI-0.5 이하의 pH 설정, EDC/NHS 신선도 체크 |
| Kinetic Distortion | Mass Transport Limitation (MTL) | Flow Rate 증가(>30µL/min), 리간드 고정 농도 하향 조절 |
데이터 신뢰도를 높이는 3단계 최적화 공정
1단계: 광학계 점검 및 베이스라인 안정성 확보
먼저 장비 전원을 켠 후, 칩을 장착하기 전(Before Chip Mounting) 단계에서 Auto Qualification Check를 실행하십시오. 이는 칩의 상태와 관계없이 장비 내부의 광학 엔진과 하드웨어가 최상의 컨디션인지 확인하는 필수 절차입니다. 특히 iMSPR과 같은 고감도 장비에서는 0.1 RU 이하의 노이즈 관리가 필수이며, 이 검사를 통과한 후에 칩을 장착(Docking)해야 합니다. 칩 장착 후에는 별도의 Automatic Chip Check를 통해 칩의 정상 안착 여부를 재확인하고, 최소 10~20분간 버퍼를 흘려 Drift(기준선의 기울어짐)가 분당 0.5 RU 이하로 떨어지는지 점검하십시오.
🧪 Pro-tip: 연구 현장 실무 꿀팁
재생 용액(Regeneration Solution) 선정 시, 처음부터 강한 산/염기를 쓰지 마세요. Glycine-HCl pH 2.0부터 단계적으로 테스트하여 리간드의 활성이 유지되는 최적의 pH를 찾는 Regeneration Scout 과정이 데이터 재현성을 결정짓습니다.
2단계: 비특이적 결합(NSB) 및 매트릭스 효과 제거
Reference Channel(Fc1)에서 신호가 높게 나온다면 NSB를 의심해야 합니다. 버퍼에 0.05% Tween-20이나 0.1 mg/mL BSA를 첨가하면 소수성 상호작용에 의한 비특이적 결합을 80% 이상 억제할 수 있습니다 (Nicoya Lifesciences, 2020).
자주 묻는 질문 (FAQ)
Q1. 데이터에 날카로운 스파이크(Spikes)가 너무 많이 발생합니다. 어떻게 하나요?
A: 대부분 버퍼 내에 녹아있던 미세 기포가 유로 안에서 터지면서 발생하는 현상입니다. 모든 버퍼는 0.22µm 필터링 후 반드시 공기를 빼주는 기포 제거(Degassing) 과정을 거쳐야 하며, 장비 내부의 기포 제거 장치(Degasser)가 정상인지 확인하세요.
Q2. 리간드 고정화(Immobilization) 수치가 너무 낮습니다.
A: pH Scouting이 선행되었는지 확인하세요. 리간드의 pI 값보다 0.5~1.0 낮은 pH 버퍼(보통 Sodium Acetate)를 사용하여 정전기적 인력을 극대화해야 합니다. 이것이 SPR 분석 트러블슈팅의 기본입니다.
Q3. 분석 후 데이터 피팅(Fitting)이 잘 안 됩니다.
A: Mass Transport Limitation 때문일 가능성이 큽니다. 리간드 농도를 낮추거나 Flow rate를 30~50µL/min으로 높여 확산 속도에 의한 간섭을 줄여보세요.
참고문헌
- Creative Biolabs. (n.d.). Surface Plasmon Resonance Protocol & Troubleshooting. Retrieved from https://www.creative-biolabs.com
- iCluebio. (2024). iMSPR 실험 최적화 체크리스트 및 트러블슈팅 가이드. iCluebio Technical Support Document.
- Myszka, D. G. (1999). Improving biosensor analysis. Journal of Molecular Recognition, 12(5), 279-284. https://doi.org/10.1002/(SICI)1099-1352(199909/10)12:5<279::AID-JMR473>3.0.CO;2-3
- NanoTemper. (2020, July 23). 4 SPR assay problems that can be resolved by improving protein quality. NanoTemper Blog.
- Nicoya Lifesciences. (2020, December 10). 4 Ways To Reduce Non-specific Binding in Surface Plasmon Resonance Experiments. Nicoya Blog.
- Sartorius. (2022). Octet SPR Analysis User Guide (Revision B). Sartorius Lab Instruments GmbH & Co. KG.
- SPR-Pages. (n.d.). Baseline drift & Validation of fitting results. Retrieved from https://www.sprpages.nl
마치며: 신뢰할 수 있는 데이터로 가는 길
SPR 분석 트러블슈팅은 장비의 성능보다는 ‘샘플과 버퍼의 준비 상태’에 의해 결정됩니다. 오늘 정리해 드린 체크리스트와 전문 문헌들을 참고하여 실험 조건을 점검하신다면 논문의 신뢰도를 한 차원 높일 수 있을 것입니다. 추가적인 기술 지원이나 장비 PQ 서비스가 필요하시다면 전문 기술팀의 조언을 받는 것도 좋은 방법입니다.