핵심요약 (Summary)
성공적인 SPR 분석 리간드 고정은 단백질의 pI보다 0.5~1.0 낮은 pH에서 정전기적 농축을 유도하는 pH Scouting 결과에 의해 결정됩니다. 실험 목적에 따라 Amine Coupling과 Capture 방식을 선택하되, Mass Transport Limitation을 방지하기 위해 50~300 RU 수준의 저밀도 고정화 전략을 수립하는 것이 데이터 신뢰성 확보의 핵심입니다.
분명 매뉴얼대로 EDC/NHS를 혼합하여 칩을 활성화하고 리간드를 주입했음에도 불구하고, Response Unit(RU) 수치가 오르지 않아 당황하신 적이 있습니까? 바이오 벤처 연구원이나 석/박사 과정 대학원생들이 SPR(Surface Plasmon Resonance) 실험에서 가장 먼저 맞닥뜨리는 장벽은 바로 SPR 분석 리간드 고정 단계의 불확실성입니다.
실무 연구원을 위한 Pro-tip: 베이스라인의 노이즈 분석
고정화 단계에서 RU 수치가 계단식으로 상승하지 않고 지그재그로 요동치거나(Noise), 일정한 방향성 없이 흐르는(Drift) 현상은 리간드의 농도 부족보다는 화학적 환경(Buffer)의 부적합성일 확률이 90% 이상입니다.
리간드 고정의 실패는 단순한 시간 낭비를 넘어, 이후 진행되는 모든 Kinetics 분석 결과의 신뢰도를 무너뜨립니다. 본 가이드에서는 2026년 최신 연구 트렌드를 반영하여, 데이터 퀄리티를 수직 상승시킬 수 있는 SPR 분석 리간드 고정 최적화 전략을 정리합니다.
1. 성공적인 SPR 분석 리간드 고정을 위한 3가지 핵심 실패 원인
실험 현장에서 발생하는 고정화 실패 사례의 약 85%는 기술적인 세부 설정 오류에서 기인합니다.
- 부적절한 pH 설정: 리간드가 칩 표면의 덱스트란 매트릭스(Dextran Matrix)로 유도되지 못하는 가장 큰 원인입니다.
- 리간드 방향성(Orientation) 이슈: Amine Coupling 시 활성 부위가 칩 바닥을 향하게 고정되면 분석 물질(Analyte)과의 결합 효율이 20% 이하로 급감합니다.
- 과도한 고정 밀도: 너무 많은 리간드를 고정하면 Mass Transport Limitation이 발생하여 정확한 k_a, k_d 분석이 불가능해집니다.
2. pH Scouting: SPR 분석 리간드 고정 성공의 열쇠
pH Scouting은 고정화의 성패를 가르는 가장 중요한 단계입니다. 칩 표면은 음전하를 띠므로, 리간드는 반드시 양전하(+)를 띠어야 정전기적으로 끌려옵니다.
최적 pH 선정을 위한 수치 가이드
- 이론적 기초: 리간드의 pI(등전점) 확인 후, pI – 0.5 ~ 1.0 수준의 pH 버퍼를 사용하십시오.
- 예시: 단백질의 pI가 6.0인 경우, pH 5.0 또는 5.5의 Acetate 버퍼에서 농축 효율이 최대화됩니다.
- Scout Run 방법: 활성화를 시키지 않은 상태에서 pH 4.0, 4.5, 5.0, 5.5 조건을 각각 120초간 주입하여 RU 상승폭이 가장 가파른 지점을 선택합니다.
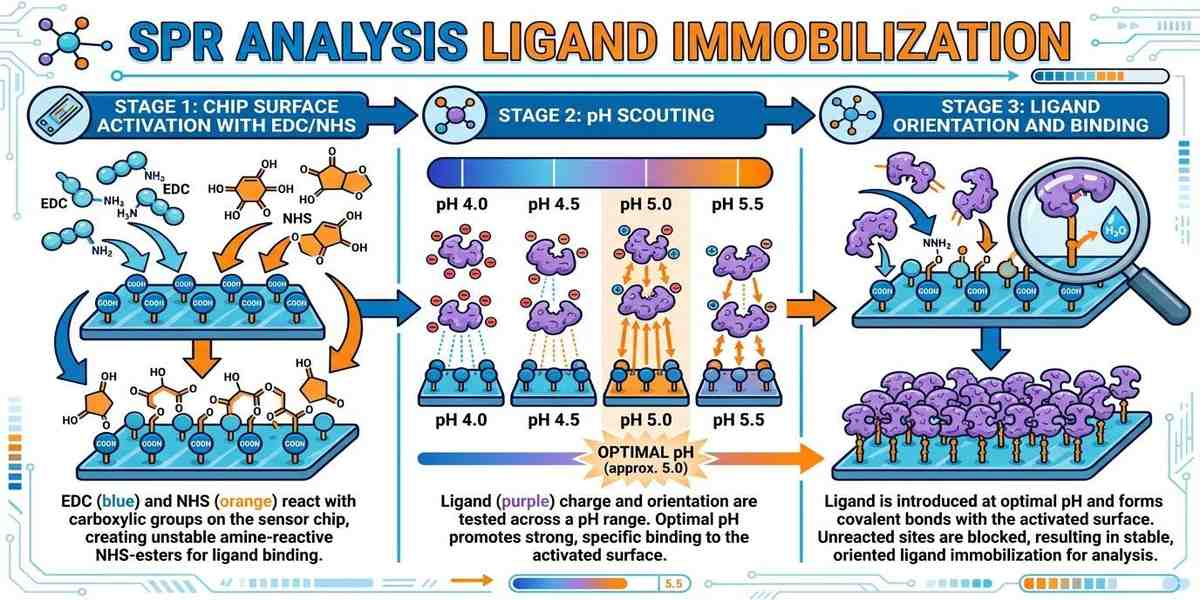
[이미지 1] SPR ANALYSIS LIGAND IMMOBILIZATION 단계별 최적화 공정
3. Amine Coupling vs Capture 방식 기술 비교
실험의 목적(Screening vs Kinetics)에 따라 최적의 고정화 방식이 다릅니다.
| 비교 지표 | Amine Coupling (공유결합) | Capture 방식 (친화결합) |
|---|---|---|
| 결합 안정성 | 매우 높음 (비가역적) | 중등도 (재생 가능) |
| 방향성 제어 | 랜덤 (Random) | 정밀 제어 가능 (Site-specific) |
| 적용 대상 | Tag 없는 단백질, 저분자 화합물 | IgG, His-tagged 단백질 |
| 데이터 품질 | 높은 RU 확보 유리 | 균일한 결합 부위 노출 유리 |
4. 정밀 Kinetics를 위한 Rmax 및 Target RU 계산
무조건 많이 붙이는 것이 좋은 데이터로 이어지지 않습니다. 1:1 결합 모델에서 이상적인 분석을 수행하려면 다음 수치를 목표로 해야 합니다.
이론적 최대 결합값 (Rmax) 공식
Rmax = (Analyte MW / Ligand MW) x Target RU x Valency
* Kinetics 분석 추천: 50 ~ 250 RU 고정
* Screening 분석 추천: 500 ~ 2000 RU 고정
5. 실전 트러블슈팅: RU가 상승하지 않을 때 체크리스트
- EDC/NHS 활성도 확인: 활성화 단계에서 칩 표면에 150~300 RU의 상승이 나타나지 않는다면 시약의 품질 저하를 의심하십시오. (분주 후 -20도 보관 필수)
- 버퍼 내 염(Salt) 농도: 10mM Acetate 버퍼에 NaCl 등의 염이 포함되어 있으면 정전기적 유도를 방해합니다. 저농도 버퍼 사용이 필수적입니다.
- 에탄올아민(Ethanolamine) 블로킹: 비특이적 결합을 제거하기 위해 1M Ethanolamine (pH 8.5)을 최소 7분(420초) 이상 흘려주어야 합니다.
핵심 용어 정리 (Glossary)
- Response Unit (RU): SPR 센서 표면에서 발생하는 굴절률 변화를 나타내는 단위로, 1 RU는 약 1 pg/mm_2의 단백질 결합을 의미합니다.
- Mass Transport Limitation: 리간드 밀도가 너무 높아 분석 물질의 결합 속도가 확산 속도에 의해 제한되는 현상으로, Kinetics 상수의 왜곡을 초래합니다.
- pI (Isoelectric Point): 분자의 알짜 전하가 0이 되는 pH 지점입니다.
자주 묻는 질문 (FAQ)
Q1. 단백질이 산성 조건에서 변성(Denature)된다면 어떻게 하나요?
A. Amine Coupling 대신 중성 pH에서 수행 가능한 Capture 방식(Streptavidin-Biotin 또는 NTA-His tag)을 사용하거나, 방향성을 유지하며 공유결합을 유도하는 ‘Capture Coupling’ 하이브리드 전략을 사용하십시오.
Q2. 칩을 재사용하기 위한 가장 안전한 방법은 무엇인가요?
A. Glycine-HCl (pH 2.0) 또는 50mM NaOH와 같은 재생 용액을 사용하되, 리간드의 결합 활성도가 10% 이상 감소한다면 재생 조건을 완화하거나 새로운 칩을 사용하는 것이 좋습니다.
참고문헌
- icluebio: SPR Principles and Technical Application Note (https://www.icluebio.com)
- Nicoya Life: SPR Sensor Selection & Optimization Guide 2024
- SPR-Pages: Immobilization Theory & Ligand Coupling Procedures
- Creative Proteomics: Troubleshooting Tips for SPR Experiments
문의 QR 코드 (메시지 연결)