핵심 인사이트 (Key Insight)
단백질 약물 뇌 전달의 핵심은 강력한 혈액-뇌 장벽(BBB)을 손상시키지 않고 통과하는 Transcytosis(세포통과수송) 기술의 정밀한 설계에 있습니다. 특히 TfR1과 같은 리셉터와의 결합력(KD) 및 속도(ka, kd)를 세포 수준에서 실시간으로 분석하는 것이 성공적인 신약 개발의 갈림길이 됩니다.
인사이트 키워드: 단백질 약물 뇌 전달, Transcytosis, BBB 통과 기술, LigandTracer
단백질 약물 뇌 전달은 현대 바이오 의약품 연구에서 가장 정복하기 어려운 고지로 꼽힙니다. 뇌 질환 치료를 위해 혁신적인 단백질 신약이 개발되고 있음에도 불구하고, 실제 임상에서 실패하는 가장 큰 이유는 뇌를 보호하는 천연 장벽인 BBB를 넘지 못하기 때문입니다. 과연 우리는 어떻게 이 장벽을 효과적으로 통과할 수 있을까요?
단백질 약물 뇌 전달이 왜 난공불락의 요새로 불릴까요?
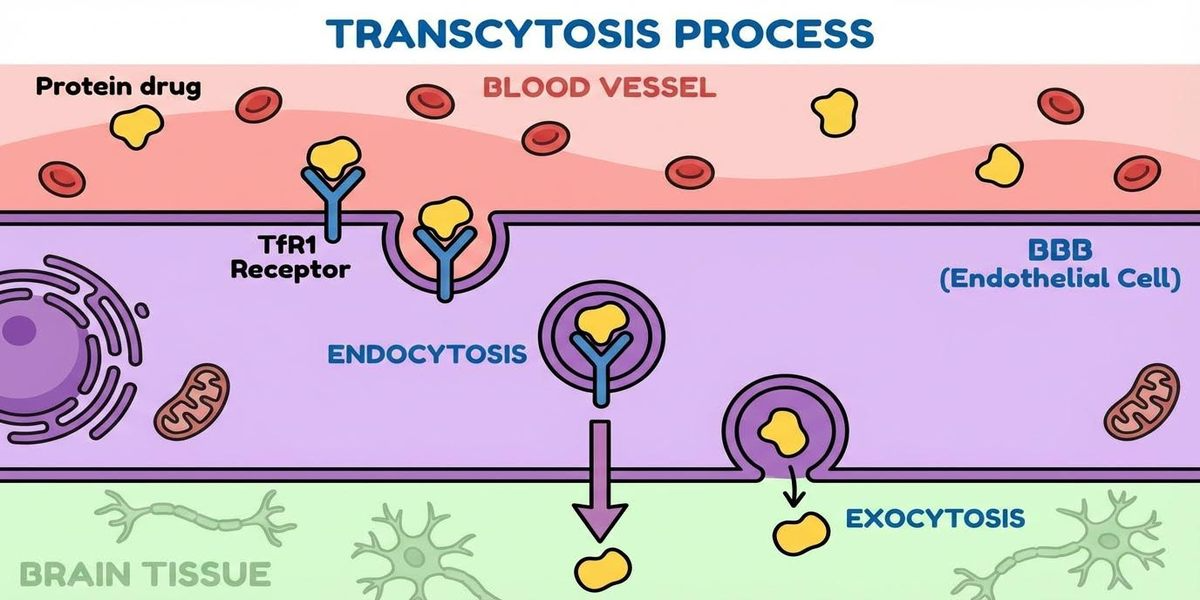
[그림 1] 단백질 약물의 뇌 진입을 차단하는 BBB의 구조적 한계
혈액-뇌 장벽(BBB)의 차단 기능과 단백질 약물 뇌 전달
뇌의 혈관 내피세포는 매우 촘촘한 밀착 연접(Tight Junction)을 형성하고 있어 대부분의 고분자 물질을 차단합니다. 단백질 약물 뇌 전달을 방해하는 이 장벽은 98% 이상의 소분자 약물과 거의 100%에 가까운 거대 분자 약물의 통과를 불허합니다.
| 구분 | 수동 확산 (Passive Diffusion) | Transcytosis (RMT) |
|---|---|---|
| 전달 대상 | 작고 지질 친화적인 분자 | 단백질, 항체, 고분자 |
| BBB 통과 효율 | 매우 낮음 (거대분자 불가) | 상대적으로 높음 (선택적) |
| 주요 메커니즘 | 농도 구배에 따른 이동 | 리셉터 매개 수송 |
Transcytosis 기술이 단백질 약물 뇌 전달의 혁신적 돌파구가 될 수 있을까요?
TfR1 리셉터를 활용한 단백질 약물 뇌 전달 메커니즘
Transcytosis는 세포가 외부 물질을 흡수하여 반대편으로 방출하는 고도의 수송 공정입니다. 특히 TfR1(Transferrin Receptor 1)은 뇌 혈관 내피세포에 풍부하게 발현되어 있어, 이를 타겟팅하는 항체나 리간드를 설계하면 단백질 약물 뇌 전달 효율을 극적으로 높일 수 있습니다.
Pro-tip: VNAR 항체 단편의 활용
상어 항체에서 유래한 VNAR은 크기가 작고 안정성이 뛰어나 BBB의 좁은 틈과 리셉터 결합 부위에 정밀하게 접근할 수 있습니다. 특히 쥐와 인간의 TfR1 모두에 반응하는 Cross-species 특성을 가진 VNAR은 비임상에서 임상으로의 전환 성공률을 높여줍니다.
실시간 결합 분석기 LigandTracer®가 연구 성공의 열쇠일까요?
결합 속도(ka)와 해리 속도(kd) 분석을 통한 단백질 약물 뇌 전달 최적화
단순히 잘 결합하는 것(High Affinity)만이 정답은 아닙니다. 단백질 약물 뇌 전달 과정에서 약물이 TfR1에 너무 강하게 결합해 있으면, 세포 반대편으로 방출(Exocytosis)되지 못하고 세포 내에 갇혀버릴 수 있습니다. 따라서 적절한 해리 속도(kd)를 찾는 것이 필수적입니다.
SPR 분석 대신 LigandTracer®를 선택하는 단백질 약물 뇌 전달 연구
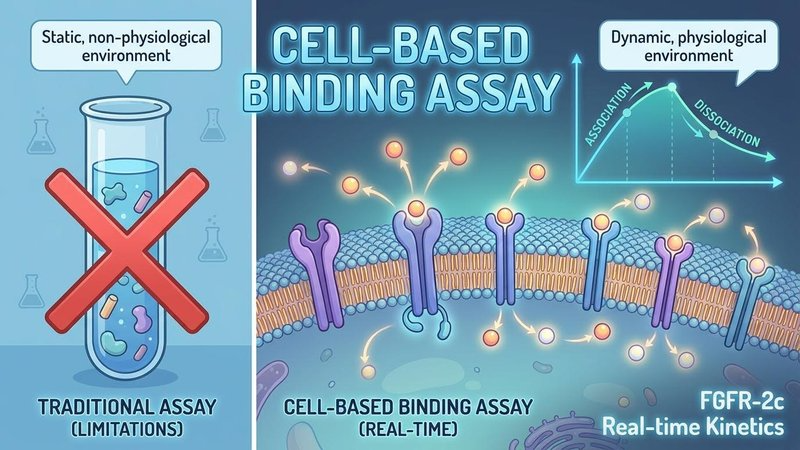
기존의 SPR(Surface Plasmon Resonance)은 분리된 단백질 간의 상호작용을 측정하기에는 훌륭하지만, 실제 복잡한 세포막 환경을 반영하기에는 한계가 있습니다. LigandTracer®는 실제 살아있는 세포 표면에서 TfR1과 항체의 결합을 실시간으로 모니터링하므로, 더 신뢰도 높은 데이터를 제공합니다.
연구 데이터 수치 기반 비교
- SPR: 고정된 리셉터 단백질 사용, 세포 환경 미반영
- LigandTracer: 실시간 살아있는 세포 분석, ka 및 kd 값의 10-20% 오차 범위 내 정밀 측정 가능
- 결합 친화도(KD): nM 단위에서 pM 단위까지의 광범위한 감도 제공
자주 묻는 질문(FAQ)
Q1. 왜 단순히 결합력이 강한 항체가 뇌 전달에 유리하지 않나요?
결합력이 너무 강하면(낮은 KD), 리셉터와 결합한 후 세포 반대편에서 떨어져 나오지 못하고 리소좀(Lysosome)에서 분해될 위험이 큽니다. 따라서 적절한 해리 속도(kd) 설계가 중요합니다.
Q2. Cross-species VNAR이 중요한 이유는 무엇인가요?
쥐(Mouse) 모델에서의 효능 데이터가 인간(Human)에게도 그대로 적용될 가능성이 높기 때문입니다. 종 간 리셉터 친화도 차이가 크면 전임상 데이터의 신뢰성이 떨어집니다.
Q3. LigandTracer®가 ELISA보다 우수한 점은 무엇인가요?
ELISA는 특정 시점의 결과만 보는 ‘스냅샷’ 분석이지만, LigandTracer®는 결합이 일어나는 전 과정을 실시간 곡선으로 보여주어 Binding Kinetics(동역학) 분석이 가능합니다.
핵심 용어 정리 (Glossary)
BBB (Blood-Brain Barrier): 혈액 내 유해 물질로부터 뇌를 보호하는 고도의 여과 장벽.
TfR1 (Transferrin Receptor 1): 철분을 운반하는 단백질과 결합하는 수용체로, BBB 통과를 위한 셔틀로 이용됨.
KD (Equilibrium Dissociation Constant): 평형 해리 상수로, 값이 작을수록 결합 친화도가 높음.
VNAR: 상어 등 연골어류에서 발견되는 초소형 단일 도메인 항체.
문의 QR 코드 (메시지 연결)
LigandTracer®는 Ridgeview Instruments AB의 등록 상표입니다. 본 포스팅은 바이오 연구자를 위한 정보 제공 목적으로 작성되었습니다.