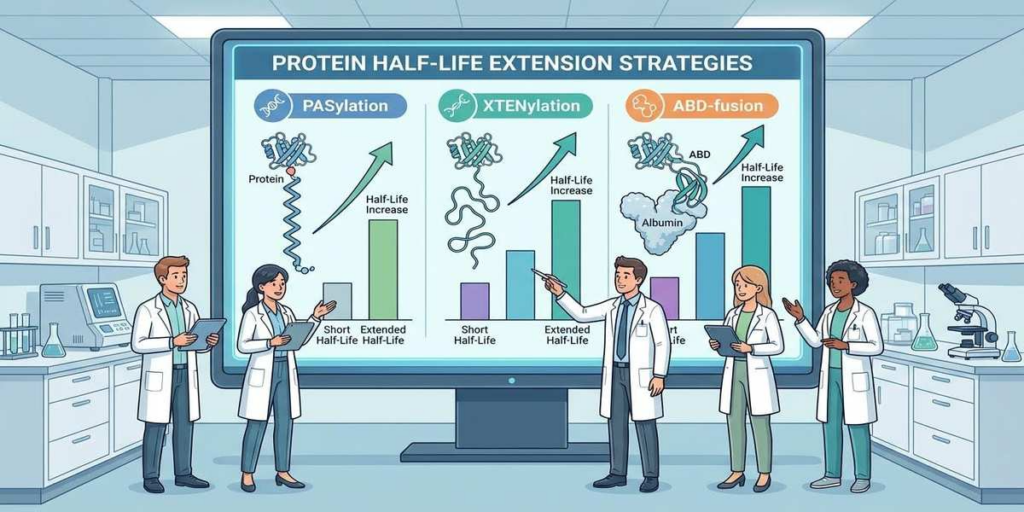
핵심 인사이트 (Key Insight)
소형 단백질 약물의 단백질 약물 반감기 연장을 위해 PASylation, XTENylation, ABD 기술이 활용되며, 각 기술은 약물의 유체역학적 반경을 넓히거나 혈중 알부민을 이용해 신장 여과를 억제합니다. 연구 결과, ABD(알부민 결합 도메인) 기술이 반감기 연장과 동시에 다른 기술 대비 60~160% 높은 종양 내 흡수율을 보여 가장 우수한 효율을 증명했습니다.
인사이트 키워드: 단백질 약물 반감기 연장, ABD 결합, 종양 흡수율, 약동학 최적화
단백질 약물 반감기 연장 기술은 현대 바이오 의약품 개발에서 소형 단백질의 한계를 극복하기 위한 필수적인 공정입니다. 특히 분자량이 60~70kDa 이하인 소형 단백질은 신장의 여과 장벽을 통과하여 빠르게 배설되기 때문에, 이를 지연시키기 위한 혁신적인 엔지니어링이 요구됩니다.
소형 단백질 약물의 빠른 제거, 어떻게 해결할 수 있을까?
치료용 단백질은 우수한 표적 결합력을 가졌음에도 불구하고, 체내 순환 시간이 짧아 투여 빈도가 잦아지는 단점이 있습니다. 이를 해결하기 위해 아미노산 서열을 변형하거나 특정 도메인을 융합하는 방식이 사용됩니다. 대표적으로 프롤린, 알라닌, 세린으로 구성된 PASylation과 음전하를 띠는 XTENylation, 그리고 혈중 알부민과 결합하는 ABD 방식이 있습니다.
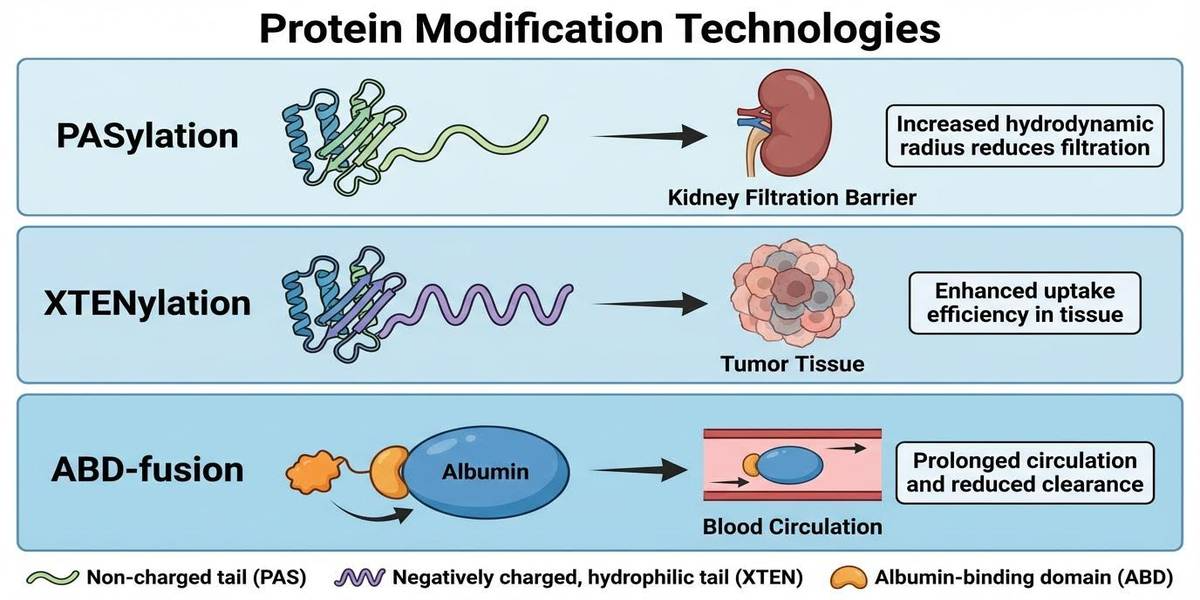
그림 1. PASylation, XTENylation, ABD 기술의 체내 작용 기전 비교
각 연장 기술의 성능 지표는 어떻게 다를까?
연구 데이터에 따르면 HER2 표적 affibody 약물에 각 기술을 적용했을 때, 물리화학적 특성과 약동학적(PK) 데이터에서 뚜렷한 차이가 관찰되었습니다. 아래 표는 각 기술별 반감기 연장 수치와 특징을 요약한 것입니다.
| 기술 구분 | 구성 요소 | 반감기 (시간) | 특징 |
|---|---|---|---|
| PAS300 | Pro, Ala, Ser (300aa) | 7.3h | 비전하, 높은 용해성 |
| PAS600 | Pro, Ala, Ser (600aa) | 11.6h | 유체역학적 반경 극대화 |
| XTEN576 | Ala, Pro, Ser, Thr, Gly, Glu | 8.7h | 음전하, 생분해성 |
| ABD Fusion | Albumin Binding Domain | 9.0h | 최고의 종양 흡수율 |
반감기보다 중요한 종양 대 정상 장기 비율의 가치는?
단순히 혈중에 오래 머무는 것보다 중요한 것은 약물이 종양에 얼마나 선택적으로 축적되느냐입니다. 종양 및 정상 장기 비율 분석 결과, ABD 결합체는 PAS나 XTEN 방식보다 종양 내 약물 농도가 현저히 높았습니다. 이는 약물의 치료 효율을 높이고 정상 조직의 부작용을 줄이는 핵심 지표가 됩니다.
Pro-tip: 연구 실무 팁
소형 약물의 PK 설계 시, 무조건적인 반감기 연장보다는 표적 조직으로의 침투력을 고려해야 합니다. PASylation은 유체역학적 반경을 크게 키워 신장 배설을 막지만, 조직 침투에는 방해가 될 수 있습니다. 반면 ABD는 상대적으로 크기가 작으면서도 알부민을 매개로 하여 효율적인 종양 축적을 유도합니다.
LigandTracer를 통한 실시간 세포 결합 분석의 역할은?
연구진은 LigandTracer 기술을 활용하여 HER2 발현 SKOV3 세포와 약물 결합체 간의 상호작용을 실시간으로 측정했습니다. 이를 통해 평형 해리 상수(KD)를 산출하고, 약물 설계 변경이 실제 세포 결합 친화도에 미치는 영향을 정확히 평가할 수 있었습니다. 특히 Interaction Map 분석은 상호작용의 이질성을 파악하는 데 결정적인 데이터를 제공했습니다.
자주 묻는 질문(FAQ)
Q1: PASylation과 XTENylation의 가장 큰 차이점은 무엇인가요?
PASylation은 전하를 띠지 않는(Non-charged) 아미노산 서열을 사용하여 용해성을 높이는 반면, XTENylation은 음전하를 띠며 생분해성이 뛰어난 특징이 있습니다. 두 기술 모두 유체역학적 반경을 넓혀 신장 여과를 방지합니다.
Q2: ABD 기술이 종양 흡수율이 더 높은 이유는 무엇인가요?
ABD는 체내에 풍부한 알부민과 결합하여 신장 배설을 피하면서도, PAS나 XTEN과 같이 거대한 폴리펩타이드 사슬을 직접 달고 있지 않아 종양 조직으로의 확산과 침투가 상대적으로 유리하기 때문으로 분석됩니다.
Q3: 신장 여과의 분자량 한계는 어느 정도인가요?
일반적으로 약 60~70kDa 이하의 단백질은 신장에서 쉽게 여과됩니다. 반감기 연장 기술은 물리적인 크기(유체역학적 반경)를 이 한계치 이상으로 “느껴지게” 만들어 체내 체류 시간을 늘립니다.
핵심 용어 정리 (Glossary)
- 유체역학적 반경 (Hydrodynamic Radius): 분자가 용액 내에서 움직일 때 나타내는 효과적인 크기입니다.
- ABD (Albumin Binding Domain): 혈중 알부민과 높은 친화도로 결합하는 작은 단백질 도메인입니다.
- 평형 해리 상수 (KD): 수용체와 리간드 사이의 결합 세기를 나타내며, 수치가 낮을수록 친화도가 높음을 의미합니다.
문의 QR 코드 (메시지 연결)
참고 문헌: Zhang, J., et al. (2024). Half-life extension via ABD-fusion leads to higher tumor uptake of an affibody-drug conjugate compared to PAS- and XTENylation. Journal of Controlled Release, 370, 468–478.
본 포스팅에 언급된 상표권 및 기술명은 해당 소유권자에게 있으며, 분석 서비스와 관련된 상세 내용은 와이클루바이오 홈페이지를 참조하시기 바랍니다.