성공적인 고순도 단백질 정제 기술은 단순히 불순물을 제거하는 것을 넘어, 3단계 전략(Capture-Intermediate-Polishing)을 통해 정제 수율 향상과 단백질 활성 유지 사이의 완벽한 균형을 찾는 과정입니다. 본 가이드는 최종 순도 95% 이상, 수율 70-90% 달성을 위한 실무 최적화 방안을 제시합니다.
고순도 단백질 정제 기술: 왜 수율과 활성인가?
바이오 의약품 개발이나 기초 학문 연구에서 고순도 단백질 정제 기술은 실험의 성패를 가르는 기초이자 핵심입니다. 순도가 높더라도 활성이 상실된 단백질은 데이터의 신뢰성을 무너뜨리며, 수율이 낮으면 연구 비용 상승과 대량 생산의 걸림돌이 됩니다. (Alpha-Lifetech, 2024) 효율적인 정제 전략은 각 단계의 물리화학적 특성을 극대화하여 손실을 최소화하는 데 있습니다.
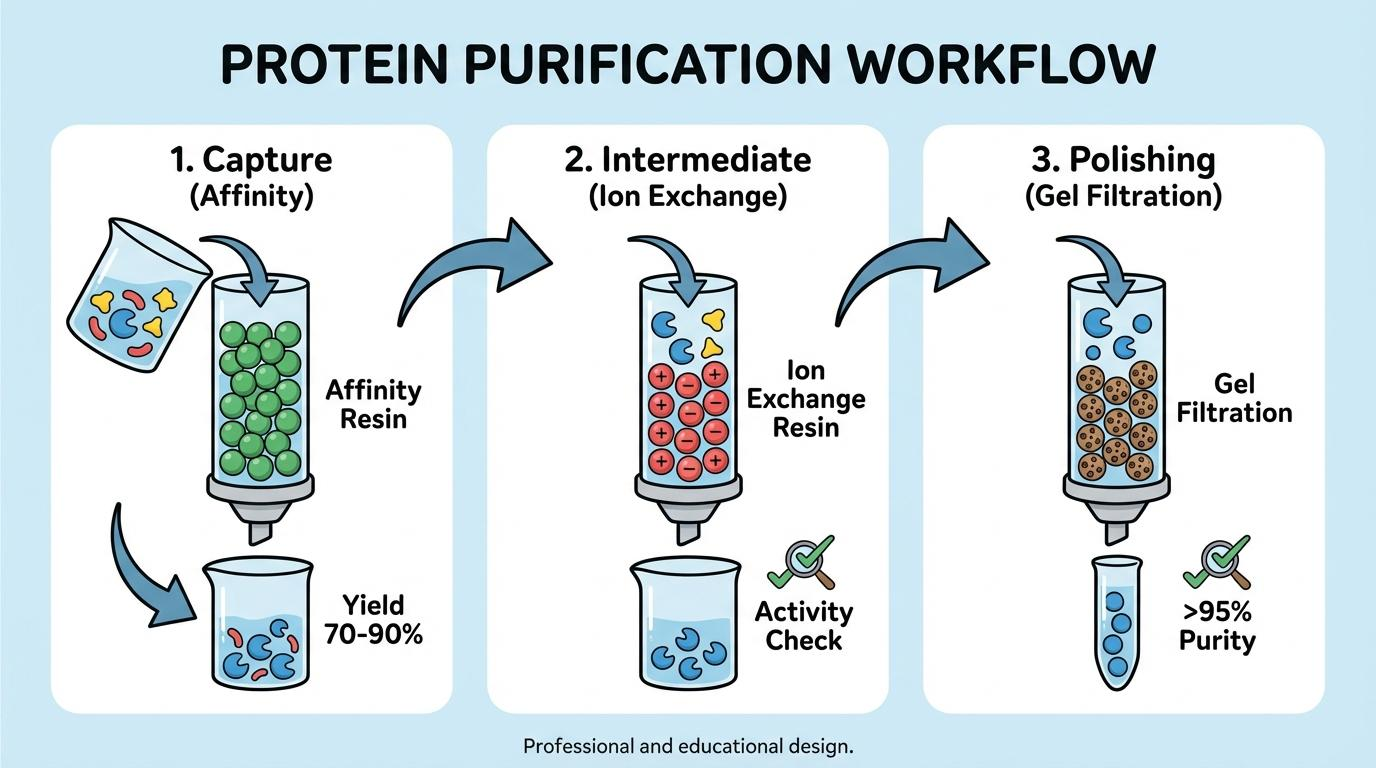
[그림 1.] 고순도 확보를 위한 표준 3단계 정제 공정
단계별 단백질 Purification 방법
단백질의 특성(Charge, Size, Hydrophobicity, Affinity)에 따라 적절한 기법을 배치하는 것이 전략의 핵심입니다.
| 정제 단계 | 주요 방법 | 주요 목적 |
|---|---|---|
| Capture (포획) | 친화성 크로마토그래피 (Affinity) | 목표 단백질 80% 이상 신속 포획 및 농축 |
| Intermediate (중간) | 이온 교환 (IEX) / 소수성 (HIC) | 유사 불순물 제거 및 순도 향상 |
| Polishing (마무리) | 크기 배제 (SEC/겔 여과) | 응집체 제거 및 최종 안정화 (>95% 순도) |
정제 수율 향상을 위한 실무 전략
정제 수율은 각 단계 회수율의 곱으로 결정됩니다. 예를 들어, 3단계 공정에서 각 단계 수율이 90%라면 최종 수율은 약 73% (0.9 x 0.9 x 0.8 = 약 0.729)가 됩니다.
🛠️ 수율 극대화를 위한 연구원 Pro-tip
- 추출 단계: 프로테아제 억제제 1x 첨가 및 초음파 파쇄 시 저온 유지 필수
- 안정성 확보: 단백질 안정화 버퍼(pH 7-8, 150mM NaCl) 최적화
- 농축 전략: 단계 간 희석을 최소화하기 위해 한외여과(Ultrafiltration) 적극 활용
단백질 활성 유지를 위한 핵심 지표
정제의 성공은 ‘양’이 아닌 ‘질’에 있습니다. 정제 과정에서 특정 활성(Specific Activity)이 증가하는지 모니터링해야 합니다.
실전 계산 사례: 특정 활성 배수 확인
초기 세포 Lysate 100mg에서 총 활성이 1,000 Units일 때 (특정 활성 = 10 U/mg)
최종 정제 후 72.7mg에서 총 활성이 1,454 Units라면? (특정 활성 = 20 U/mg)
➔ 결과: 특정 활성이 2배 증가하였으므로 활성 유지 및 정제 성공 확인!
전문 용어 정리 (Glossary)
단위 단백질 질량당 활성(U/mg). 정제도가 높아질수록 이 수치가 상승합니다.
단백질 분자들이 비정상적으로 뭉치는 현상. 활성 상실의 주요 원인입니다.
염 농도나 pH를 서서히 변화시켜 목표 단백질을 컬럼에서 분리해내는 방식입니다.
단백질 분해 효소의 작용을 막아 목표 단백질의 파괴를 방지하는 첨가제입니다.
자주 묻는 질문 (FAQ)
Q1. 수율과 활성 중 무엇을 우선해야 하나요?
연구 목적에 따라 다릅니다. 구조 분석이 목적이라면 순도와 활성이 최우선이지만, 산업적 생산 단계라면 경제적인 수율 확보가 필수적입니다. 보통 70% 이상의 균형점을 찾는 것이 일반적입니다.
Q2. 겔 여과(SEC) 단계에서 샘플이 너무 희석됩니다.
SEC는 원리상 희석이 발생할 수밖에 없습니다. 이를 방지하기 위해 로딩 전 샘플 농도를 극대화하고, 정제 후 즉시 한외여과(Amicon 등)를 통해 농축하는 프로세스를 권장합니다.
문의 QR 코드 (메시지 연결)