핵심 인사이트 (Key Insight)
정밀한 3D Spheroid 결합 분석은 신약 후보 물질의 실제 효능을 예측하는 Translational pharmacology의 핵심입니다. Tumor microenvironment mimicry를 통해 구현된 In vivo-like binding kinetics 데이터는 2D 모델이 제공하지 못하는 Antibody penetration depth와 Drug retention analysis에 대한 정량적 지표를 제시하여 연구의 완성도를 결정짓습니다.
인사이트 키워드: 3D Spheroid 결합 분석, In vivo-like binding kinetics, Tumor microenvironment, Antibody penetration
왜 2D 환경에서 측정된 Affinity 데이터는 임상에서 재현되지 않을까요?
바이오 신약 개발 현장에서 3D Spheroid 결합 분석의 중요성이 대두되는 이유는 명확합니다. 전통적인 2D monolayer 방식은 모든 세포가 약물에 균일하게 노출되는 가상의 환경을 전제하기 때문입니다. 하지만 실제 종양은 높은 세포 밀도와 물리적 압력, 그리고 복잡한 ECM(Extracellular Matrix)으로 구성된 Tumor microenvironment를 형성하고 있습니다. 이러한 환경에서는 약물이 표적에 도달하기까지의 시간과 물리적 제약이 발생하며, 이는 곧 In vivo-like binding kinetics의 변화로 이어집니다.
기존 분석 모델의 치명적 한계점
- 약물 확산의 부재: 2D 모델은 확산(Diffusion) 장벽을 고려하지 않아 과대평가된 ka 값을 산출함
- 조직 모사 실패: 실제 생체 내 Tumor microenvironment mimicry가 결여되어 데이터의 신뢰도 하락
- 지표의 단순성: 단순한 KD 값만으로는 약물의 중심부 침투 능력(Penetration)을 설명할 수 없음
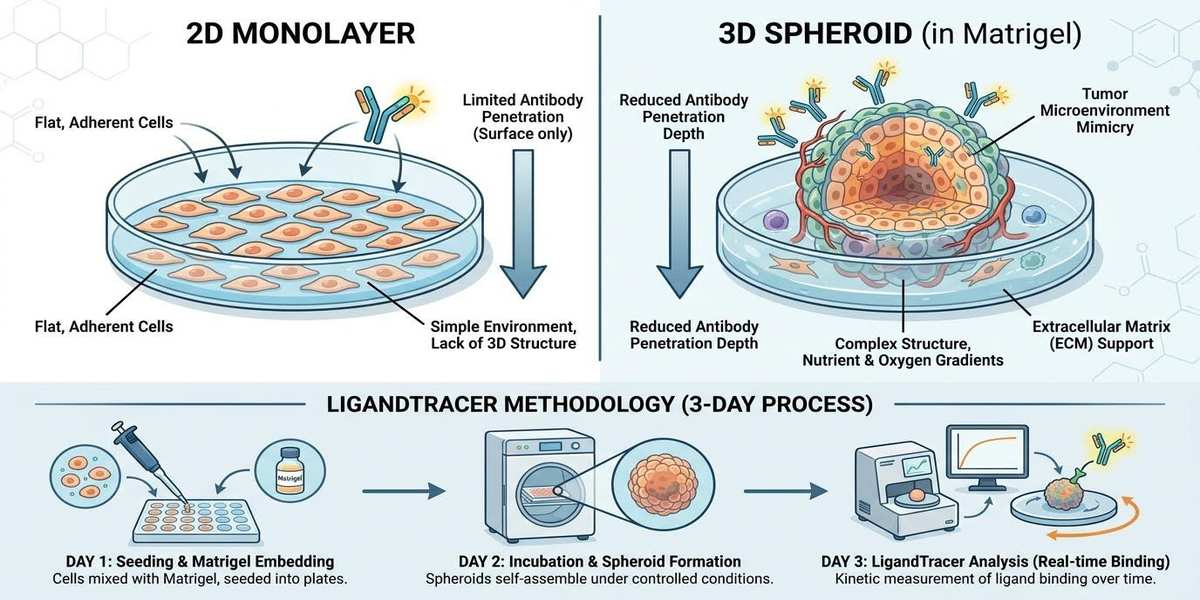
[3D Spheroid 모델 내 항체 침투 깊이와 실시간 결합 곡선의 상관관계]
성공적인 3D Spheroid 결합 분석을 위한 LigandTracer methodology란?
실제 종양과 유사한 데이터를 얻기 위해서는 입체적인 구조를 유지한 채 실시간으로 신호를 추적할 수 있는 Real-time binding assay가 필요합니다. LigandTracer methodology는 이러한 요구를 충족시키는 혁신적인 플랫폼입니다. 특히 Matrigel 1.1% 코팅을 이용한 Matrigel immobilization 기술은 스페로이드를 바닥면에 안정적으로 고정하여, 장시간의 측정 과정 중에도 데이터의 흔들림을 원천 차단합니다.
정량적 데이터 비교: 2D Monolayer vs 3D Spheroid 분석
연구자들이 Drug retention analysis를 설계할 때 반드시 고려해야 할 수치적 차이점을 비교했습니다.
| 분석 파라미터 | 2D Monolayer | 3D Spheroid (TME Mimic) |
|---|---|---|
| Apparent ka | 빠름 (단순 결합) | 완만함 (확산 포함) |
| Antibody Penetration | 분석 불가 (노출 즉시 결합) | 실시간 침투 깊이 측정 가능 |
| Retention 특성 | 세척 시 급격한 신호 감소 | 중심부 포획으로 인한 완만한 해리 |
| Kinetic Profiling | 1단계 결합 모델 | 다단계 확산-결합 모델 |
In vivo-like 데이터를 보장하는 3일 완성 실험 프로토콜
높은 재현성을 확보하기 위한 3D Spheroid 결합 분석의 핵심 단계입니다.
- Day 1 (Matrigel Preparation): 4도에서 냉각된 1.1% Matrigel을 박막 코팅합니다. 이는 Tumor microenvironment mimicry를 위한 기저층이 됩니다.
- Day 2 (Stabilization): 균일한 크기의 스페로이드를 코팅층에 배치합니다. Overnight 배양을 통해 물리적인 Matrigel immobilization을 유도합니다.
- Day 3 (Kinetic Measurement): LigandTracer를 가동합니다. AF647 형광 표지 항체와 RedNIR detector를 사용하여 노이즈가 최소화된 실시간 신호를 획득합니다.
연구원 가이드 (Pro-tip): 데이터 보정의 중요성
스페로이드의 밀도에 따라 약물 투과 속도가 달라질 수 있습니다. Kinetic profiling 시 반드시 동일한 조건에서 배양된 대조군(Monolayer) 데이터를 병행 확보하여, 순수한 3D 구조에 의한 침투 지연 효과를 분리하여 해석하십시오.
HER2/Trastuzumab 모델을 통한 Antibody penetration depth의 실질적 해석
HER2-expressing SKBR3 세포를 이용한 사례에서 Trastuzumab의 결합 거동은 매우 흥미롭습니다. 3D 모델에서 측정된 In vivo-like binding kinetics는 초기 결합 이후에도 수 시간 동안 신호가 우상향하는 독특한 패턴을 보입니다. 이는 항체가 스페로이드 외부 수용체에 포화된 후, 다시 내부의 Antibody penetration depth를 확장하며 깊숙이 침투하고 있음을 의미합니다. 이러한 Drug retention analysis 데이터는 향후 동물 실험에서의 투여 간격 설정에 결정적인 근거가 됩니다.
자주 묻는 질문 (FAQ)
Q1. 3D Spheroid 결합 분석 시 Matrigel의 농도를 조절해야 하는 이유는 무엇입니까?
Matrigel의 농도가 너무 높으면 그 자체가 물리적 장벽이 되어 리간드의 확산을 방해하고 In vivo-like binding kinetics를 왜곡할 수 있습니다. 1.1% 농도는 스페로이드를 고정하는 동시에 약물 투과를 방해하지 않는 최적의 수치입니다.
Q2. LigandTracer methodology를 사용할 때 배경 신호(Background) 문제를 어떻게 해결하나요?
원적외선(NIR) 영역의 형광체인 AF647과 전용 RedNIR detector를 조합하면 세포나 Matrigel에서 발생하는 자가 형광을 회피할 수 있습니다. 이를 통해 고감도의 Real-time binding assay 데이터를 얻을 수 있습니다.
Q3. 스페로이드 크기가 일정하지 않을 경우 데이터에 어떤 영향을 미치나요?
스페로이드의 직경은 Antibody penetration depth에 직접적인 영향을 줍니다. 크기가 일정하지 않으면 확산 시간의 편차가 커져 Kinetic profiling의 재현성이 떨어지므로, 300-400um 수준의 일정한 크기를 선별하여 사용하는 것이 권장됩니다.
핵심 연구 용어 정리 (Glossary)
- Tumor Microenvironment Mimicry: 실제 종양 내부의 물리화학적 특성(pH, 산소 농도, ECM 구성 등)을 실험실 환경에서 재현하는 기술입니다.
- Kinetic Profiling: 단순히 결합 여부를 보는 것을 넘어, 시간의 흐름에 따른 결합(ka)과 해리(kd)의 모든 동역학적 특성을 수치화하는 분석법입니다.
- In vivo-like Binding Kinetics: 복잡한 생체 조직 내부와 유사한 환경 조건에서 측정된 리간드와 수용체 간의 결합 속도 상수입니다.
바이오 분석 전문가 1:1 빠른 상담 QR
본 포스트에 수록된 분석 가이드 및 사례 연구는 전문 연구원의 검수를 거쳤으며, LigandTracer 및 Matrigel은 각 소유권자의 등록 상표임을 명시합니다.