핵심 인사이트 (Key Insight)
면역항암제 개발에서 FcγR 결합 분석은 항체의 Effector function(ADCC, CDC)을 정량적으로 예측하고 설계할 수 있는 가장 정밀한 물리화학적 지표입니다. 특히 실시간 label-free 기술인 SPR을 통한 CD16a, CD32a, CD64 수용체와의 결합 동역학(Kinetics) 데이터는 실제 세포 독성 효능(EC50)뿐만 아니라 체내 반감기 및 안전성 프로파일과도 직결되는 핵심 데이터입니다.
인사이트 키워드: FcγR 결합 분석, SPR kinetics, ADCC 효능, 면역항암제
왜 FcγR 결합 분석이 항체 치료제 개발의 성공과 실패를 결정짓는 기준이 될까요?
항체 치료제의 최종적인 치료 가치는 단순히 표적 항원(Antigen)에 결합하는 것을 넘어, 환자의 면역 시스템을 얼마나 정교하게 제어하느냐에 달려 있습니다. FcγR 결합 분석은 항체의 Fc 부위가 NK세포, 대식세포 등에 발현된 수용체와 결합하여 유도하는 항체 의존적 세포 독성(ADCC) 및 보체 활성화를 통한 세포 용해(CDC)의 강도를 결정합니다.
다양한 Fc gamma Receptor 결합 분석 방법, 우리 실험실에 가장 적합한 선택은 무엇일까요?
효과적인 항체 의약품 개발을 위해서는 분석 목적과 샘플의 특성에 따라 최적의 방법론을 선택해야 합니다. 크게 순수 단백질 간의 물리화학적 상호작용을 측정하는 비세포 기반 방법과, 실제 세포막 환경을 반영하는 세포 기반 방법으로 나뉩니다.
2.1 정밀한 물리화학적 정량: 비세포 기반 방법들 (Non-cell based)
- SPR (Surface Plasmon Resonance): 실시간 결합/해리 속도(ka, kd)와 친화도(KD)를 고정밀도로 측정합니다.
- BLI (Biolayer Interferometry): Octet과 같은 Dip-and-read 방식으로, 유체가 흐르지 않는 환경에서 Crude sample 분석이 가능하며 처리 속도가 빠릅니다.
- MST (Microscale Thermophoresis): 열 이동 현상을 이용해 용액 내에서 결합력을 측정하며, 매우 적은 샘플 양(10 uL 미만)으로 분석이 가능합니다.
- AlphaScreen / ELISA: 비드 기반 또는 플레이트 기반 분석으로, 고속 스크리닝(HTS)에 유리하며 상대적인 결합 강도(IC50/EC50) 산출에 적합합니다.
2.2 실제 생체 환경의 모사: 세포 기반 방법들 (Cell-based)
- LigandTracer: 살아있는 세포 표면에 항체가 결합하고 해리되는 과정을 실시간으로 추적하여 세포 수준의 Kinetics(ka, kd, KD)를 제공합니다.
- Flow Cytometry Binding Assay: 유세포 분석기를 활용하여 세포 표면 결합량을 형광 강도(MFI)로 측정하며, 수용체 발현 밀도가 높은 세포주 검증에 유용합니다.
- ADCC Reporter Bioassay: Jurkat-CD16a 세포 등을 활용하여 결합 이후의 신호 전달 경로 활성화를 루시페레이즈 신호로 정량화합니다.
2.3 분석 효율 극대화: 방법별 특성 및 적용 단계 비교표
| 분석 방법 | 주요 장점 | 주요 단점 | 권장 적용 단계 |
|---|---|---|---|
| SPR | 고정밀 Kinetics (ka, kd) | 샘플 정제 필요, 높은 비용 | 초기 스크리닝 ~ 개발 |
| BLI | 빠른 속도, Crude 호환성 | 낮은 감도 (저분자 취약) | 배양액 스크리닝 |
| Cell-based | 생리적 환경 반영 | 세포 컨디션에 따른 변동 | 최종 후보 검증 (MoA) |
| Reporter | 신호 전달 계측 가능 | 특정 경로로 제한됨 | Potency 평가, QC |
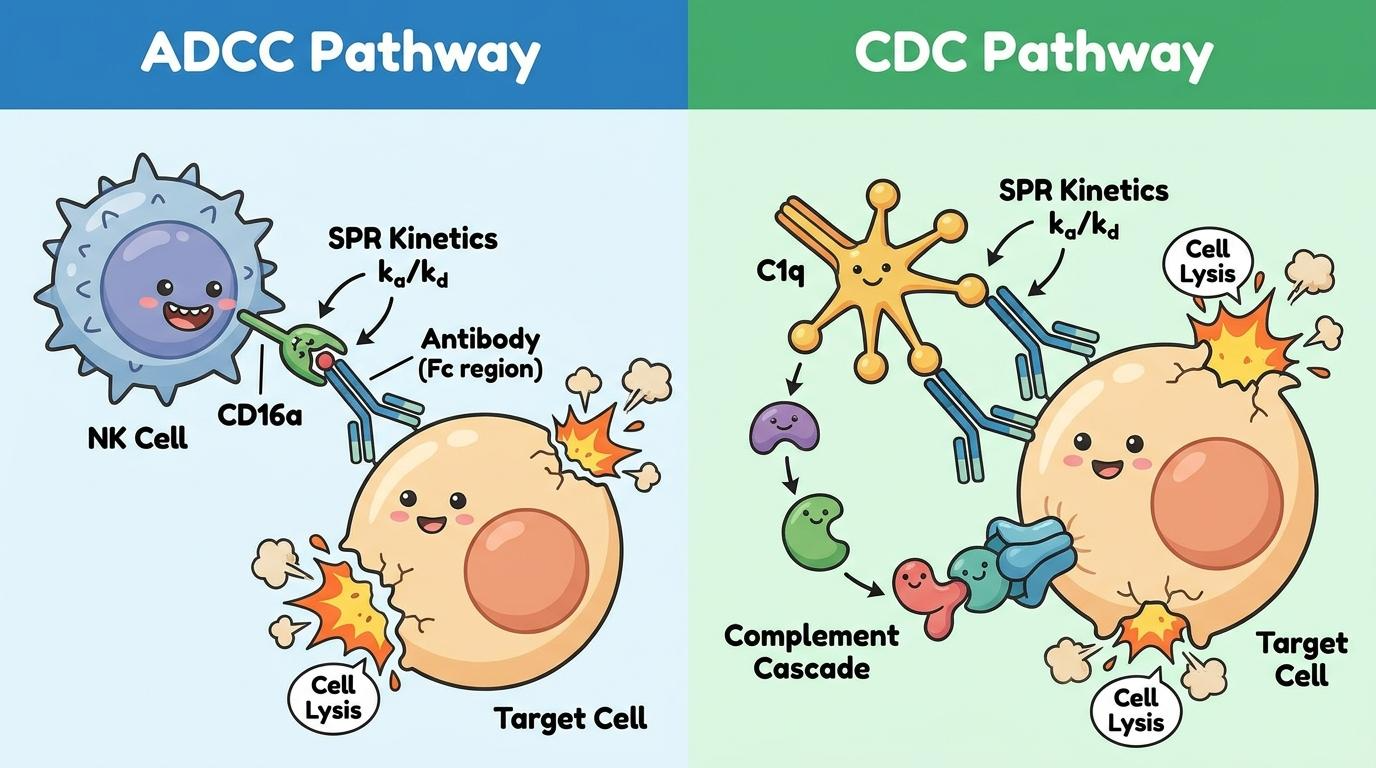
[그림 1] 항체 Fc-FcγR 복합체 형성 과정과 면역 반응 유도 메커니즘
SPR kinetics 데이터는 어떻게 실제 세포 독성 효능을 예견할 수 있을까요?
표면 플라즈몬 공명(SPR) 기술이 제공하는 ka(결합 속도)와 kd(해리 속도)는 항체가 수용체에 얼마나 빨리 붙고, 얼마나 오래 머무르는지를 보여주는 ‘동역학적 지문’입니다. 단순히 총 결합량(Affinity, KD)만 보는 것이 아니라, Residence time(1/kd)을 분석함으로써 항체가 면역 세포를 충분히 자극할 만큼 머무르는지를 파악할 수 있습니다.
실무자를 위한 Pro-tip: glycosylation 관리의 중요성
FcγR의 핵심 결합 부위인 Asn297 잔기의 당화(Glycosylation) 패턴은 SPR 결과에 막대한 영향을 미칩니다. 특히 푸코스(Fucose)가 제거된(Afucosylated) 항체는 CD16a 결합력이 비약적으로 상승합니다. 따라서 세포주 개발 단계에서부터 당화 패턴 분석과 SPR 분석을 병행하여 Critical Quality Attribute(CQA)를 관리해야 고품질의 바이오의약품 생산이 가능합니다.
3. 핵심 타겟 분석: CD16a, CD32a, CD64 수용체별 최적 지표
각 FcγR 패널은 서로 다른 면역 작용을 담당하므로, 분석 목적에 맞는 타겟팅이 필요합니다. 아래 데이터는 항체 엔지니어링 시 참고해야 할 수용체별 특성과 분석 목표치입니다.
| 대상 수용체 | 주요 Effector 세포 | 세포내 기능 | SPR KD 목표치 |
|---|---|---|---|
| CD16a (V158/F158) | NK Cell, Monocyte | ADCC 유도 (최우선) | 10 nM (V-type) |
| CD32a (H131/R131) | Macrophage, Neutrophil | 식세포 작용 (Phagocytosis) | 100 nM 미만 |
| CD64 (High Affinity) | Monocyte, Macrophage | 초기 면역 활성화 | 1 uM 미만 |
심화 Q&A: 연구자가 자주 묻는 질문
Q1. SPR 분석만으로 ADCC 효능을 100% 확신할 수 있나요?
아니요. SPR은 정제된 단백질 간의 결합력을 측정하는 2D 환경 분석입니다. 실제 세포막의 복잡한 환경이나 신호 전달 경로를 반영하기 위해 최종 단계에서는 반드시 세포 기반 Reporter Assay나 cytotoxicity assay를 병행해야 합니다.
Q2. IgG Allotype(G1, G2, G3, G4)에 따라 FcγR 분석 전략이 달라지나요?
매우 중요합니다. IgG1과 IgG3는 강한 결합력을 통해 ADCC를 활발히 유도하지만, IgG2와 IgG4는 결합력이 낮아 차단용(Blocking) 항체 개발에 주로 쓰입니다. 따라서 개발하려는 치료제의 MoA에 맞춰 적절한 Allotype 스크리닝이 선행되어야 합니다.
Q3. CDC 효능 평가 시 보체 결합력(C1q) 측정이 필수인가요?
CDC 효능을 최적화하려면 보체 시스템의 첫 단추인 C1q 결합 분석이 핵심입니다. C1q는 분자량이 매우 크고 복합적인 구조를 가지므로, 일반적인 1:1 결합 모델보다는 Bivalent 또는 Avidity 모델을 적용하여 분석해야 실제 보체 활성화 능력과 일치하는 결과를 얻을 수 있습니다.
핵심 용어 정리 (Glossary)
- FcγR (Fc gamma Receptor): 면역글로불린 G(IgG) 항체의 Fc 부위를 인식하여 면역 세포의 활성 또는 억제를 지시하는 센서 단백질.
- Kinetics (ka/kd): 분자가 결합하는 속도(association)와 떨어지는 속도(dissociation)를 정의하는 동역학 지표.
- ADCC (Antibody-Dependent Cellular Cytotoxicity): 항체가 표적세포에 결합한 후 NK세포의 수용체를 자극하여 세포를 직접 사멸시키는 기전.
- CDC (Complement-Dependent Cytotoxicity): 항체-항원 복합체에 보체(Complement)가 결합하여 막 공격 복합체(MAC)를 형성, 세포를 용해시키는 기전.
분석 상담 QR 코드 (메시지 연결)
심층 학습을 위한 연관 블로그
© All trademarks and registered trademarks mentioned are the property of their respective owners. Octet is a registered trademark of Sartorius. Biacore is a trademark of Cytiva.