핵심 인사이트 (Key Insight)
성공적인 SPR Protein Capture를 위해서는 분석 목적에 맞는 센서 칩 선택과 리간드 고정화 방식의 결정이 선행되어야 합니다. Fc Fusion 단백질의 경우, Protein A/G 칩을 사용하면 Fc fusion 단백질을 배향성 있게 고정화할 수 있어서Kinetics 분석의 데이터 신뢰도를 향상 시킬 수 방법입니다.
인사이트 키워드: SPR Protein Capture, 리간드 고정화, Protein A/G 칩, 배향성 최적화
왜 내 SPR 데이터는 매번 Rmax 값이 예상과 다르게 나올까? 라는 고민을 해보신 적이 있나요? SPR Protein Capture는 단순히 단백질을 칩에 붙이는 작업을 넘어, 리간드 단백질이 분석 물질(Analyte)과 상호작용하기 가장 좋은 상태로 ‘센서칩에 고정화’ 하는 방법입니다. 리간드의 배향이 잘못되면 아무리 정밀한 장비를 써도 분석 데이터의 신뢰도에 의문을 갖게 되는 원인이 됩니다.
SPR Protein Capture: 올바른 센서 칩 선택이 고품질 데이터를 얻기 위한 중요한 과정입니다
연구자가 실험 설계 단계에서 가장 먼저 맞닥뜨리는 질문은 “어떤 칩에 어떻게 리간드를 고정할 것인가”입니다. 리간드 고정화는 실험의 재현성을 좌우하는 첫 번째 관문입니다. 범용적인 센서 칩은 표면에 COOH를 갖고 있습니다. 여기에 리간드를 고정할 때, 공유 결합인 Amine Coupling을 선택할지, 혹은 특이적 캡처 방식인 Protein A/G 칩을 선택할지를 결정합니다. 결정에 따라 데이터의 성격이 완전히 달라질 수 있습니다.
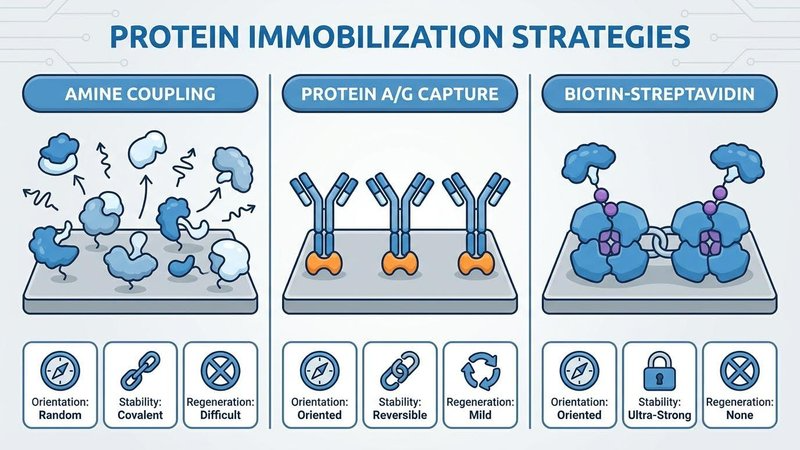
[그림 1] 리간드 배향성(Orientation)에 따른 SPR 데이터 신뢰도 차이
Amine Coupling의 명과 암: 강력한 결합 뒤에 숨겨진 무작위 배향의 함정
Amine Coupling은 리간드의 리신(Lysine) 잔기와 칩 표면을 영구적인 공유 결합으로 연결합니다. 결합의 안정성 측면에서는 최고지만, 문제는 ‘무작위성’에 있습니다. 고정화된 단백질의 활성 부위가 칩 표면을 향해 있으면, 활성부위가 가려지게 되어 비특이적 결합이 증가합니다. 즉, 실제 분석 물질과의 결합량은 줄어듭니다. 이는 특히 고순도(>95%) 단백질이 확보되지 않았을 때 Kinetics 분석을 방해하는 가장 큰 문제가 됩니다.
왜 전문가들은 Fc Fusion 단백질에 Protein A/G 칩을 추천할까요?
이러한 무작위성의 한계를 극복하는 솔루션이 바로 Protein A/G 칩입니다. Protein A/G는 Fc Fusion 단백질의 Fc 영역에만 선택적으로 결합합니다. 이를 통해 항체의 Fab 영역이나 융합된 도메인이 외부로 자유롭게 노출되도록 배향성 최적화를 이끌어냅니다. 결과적으로 일관된 Rmax 값을 얻 수 있으며, 재생(Regeneration) 과정을 통해 칩을 효율적으로 재사용할 수 있는 경제적 이점까지 제공합니다.
Protein A/G 칩: 배향성의 정점, 그러나 불가피한 리간드의 소모
Fc Fusion 단백질 분석의 표준인 Protein A/G 칩은 리간드를 일정한 방향으로 세워주는 배향성 최적화 능력이 탁월합니다. 하지만 이 방식은 매 사이클마다 재생(Regeneration) 용액을 사용하여 리간드와 분석 물질을 통째로 칩에서 떼어내는 ‘Stripping’ 과정을 거칩니다. 결과적으로 매 실험마다 리간드를 새로 주입해야 하므로, 리간드 샘플이 귀하거나 고가일 경우 비용 부담이 커지는 Pain Point가 있습니다.
Biotin-Streptavidin: 리간드 소모를 최소화하는 ‘박제형’ 고정화 전략
리간드의 소모를 획기적으로 줄이고 싶다면 Biotin-Streptavidin 시스템이 정답입니다. 이 결합은 비공유 결합 중 가장 강력한 KD 10-15 M 수준으로, 한 번 칩에 고정된 리간드는 수백 번의 재생 사이클을 거쳐도 칩에서 떨어지지 않습니다. 즉, Amine Coupling처럼 리간드를 반영구적으로 사용하면서도, AviTag(부위 특이적 비오틴화)를 활용하면 캡처 방식 특유의 완벽한 배향성까지 동시에 거머쥘 수 있습니다.
초고친화도(Ultra-high Affinity) 분석의 필수 조건: 제로-드리프트(Zero-Drift)
10-10 M 이하의 강력한 결합을 분석할 때, 리간드가 미세하게 해리되는 ‘Leakage’는 kd 값 산출에 치명적인 오차를 만듭니다. His-tag이나 Protein A/G에서 발생할 수 있는 미세한 Drift조차 허용되지 않는 정밀 Kinetics 분석에서 Biotin-SA는 가장 완벽한 리간드 고정화 상태를 제공합니다. 흔들리지 않는 Baseline은 초고친화도 분석 데이터의 신뢰도를 보장하는 유일한 길입니다.
실무자를 위한 캡처 방식별 전략적 선택 가이드
| 전략적 지표 | Protein A/G 캡처 | Biotin-SA (AviTag) | Amine Coupling |
|---|---|---|---|
| 리간드 소모량 | 많음 (매회 소모) | 매우 적음 (반영구적) | 적음 (영구적) |
| 베이스라인 안정성 | 우수 (골디락스 존) | 극한 (Drift 거의 없음) | 매우 우수 |
| 배향성 (Orientation) | 매우 우수 | 완벽 (부위 특이적) | 낮음 (랜덤) |
| 주요 적용 대상 | 일반 항체 스크리닝 | 희귀 샘플, 초고친화도 | 대량 리간드 고정화 |
His-tag 캡처의 불안정성 vs Fc Fusion의 ‘골디락스 존’
널리 쓰이는 His-tag 캡처(Ni-NTA)는 결합력이 10-5 ~ 10-6 M 수준으로 약해 실험 중 리간드가 조금씩 새어 나가는 누출(Leakage) 문제가 잦습니다. 반면 Fc-Protein A의 결합은 10-8 M 수준으로, 너무 강해서 재생이 안 되지도 않고 너무 약해서 데이터가 흔들리지도 않는 이른바 ‘골디락스 존(Goldilocks Zone)’에 해당합니다. 이것이 바로 정밀한 Kinetics 분석을 위해 Fc Fusion 포맷이 업계 표준으로 자리 잡은 이유입니다.
연구 현장 실무 팁 (Pro-tip)
성공적인 SPR Protein Capture를 위해 리간드 캡처 수준(Capture Level)을 100-500 RU 범위로 관리하십시오. 1,000 RU를 초과할 경우 Analyte와의 비정상적인 재결합(Rebinding)이나 입체 장애(Steric Hindrance)로 인해 실제 결합 상수(KD)가 왜곡될 수 있습니다. 데이터의 질은 RU의 높이가 아니라 곡선의 형태(Curvature)에서 결정된다는 점을 명심하십시오.
신뢰할 수 있는 SPR 데이터, 전문가의 설계에서 시작됩니다.
[서비스 확인] SPR 분석 위탁 프로세스 및 장비 사양[기술 가이드] Protein-Cell Binding Affinity 분석법 상세 보기
자주 묻는 질문 (FAQ)
Q1. COOH 표면 센서 칩에서 비특이적 결합이 심할 때 가장 먼저 체크할 것은?
A1. 샘플 내의 응집체(Aggregate) 유무를 SEC 등으로 먼저 확인하십시오. 그 후 러닝 버퍼에 salt, BSA, CM-Dextran, 0.005~0.1% Tween20이나 15 mM Imidazole을 추가하여 표면 전하에 의한 비특이적 결합을 상쇄하는 것이 효과적입니다.
Q2. Protein A와 Protein G 중 어떤 캡처 칩이 더 범용적인가요?
A2. 분석하고자 하는 항체의 종(Species)에 따라 다릅니다. 인간 IgG1/2/4는 Protein A에 매우 강하게 결합하지만, 마우스 IgG1은 Protein G가 더 적합합니다. 다양한 종의 항체를 다룬다면 Protein A/G 혼합 칩이 가장 범용적인 선택입니다.
Q3. His-tag 캡처 데이터를 논문에 쓰기에 무리가 있을까요?
A3. 단순한 스크리닝 용도로는 가능하지만, 정밀한 Kinetics 분석을 위해서는 캡처 안정성이 입증된 Fc Fusion이나 Biotin 방식을 권장합니다. His-tag의 Leakage는 Koff 값 산출 시 치명적인 오차를 유발할 수 있기 때문입니다.
핵심 용어 정리 (Glossary)
- SPR Protein Capture: 특정 Tag(Fc, His, Biotin 등)를 이용해 리간드를 센서 표면에 안정적으로 결합시키는 모든 과정을 의미합니다.
- 배향성 최적화 (Orientation Optimization): 분석 물질이 리간드와 결합하기 가장 좋은 방향으로 단백질을 고정하여 결합 활성을 극대화하는 기술입니다.
- Baseline Drift: 리간드의 해리나 버퍼의 온도 변화 등으로 인해 기준선이 점진적으로 상승하거나 하강하는 현상으로 데이터 왜곡의 원인이 됩니다.
- Regeneration (재생): 결합된 Analyte를 강제로 제거하여 센서 칩 표면을 리간드 캡처 전 상태로 되돌리는 과정입니다.
문의 QR 코드 (연구 설계 지원)
Biacore™는 Cytiva의 등록 상표입니다. 본 콘텐츠는 연구자들의 실험 설계 최적화를 돕기 위한 정보 제공용으로 제작되었습니다.