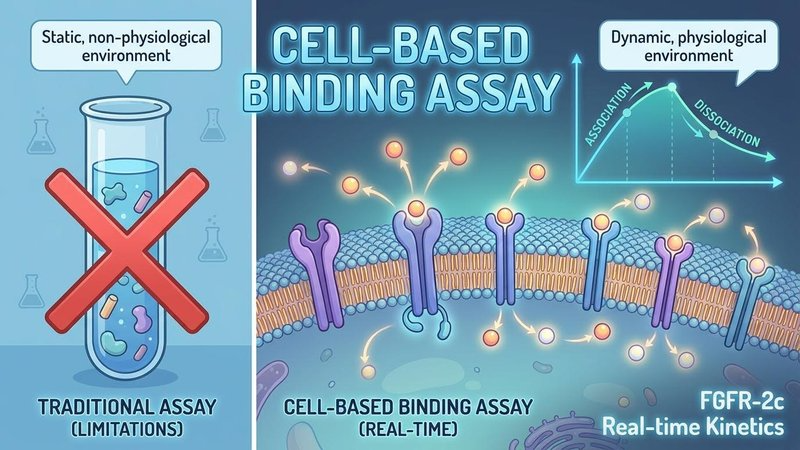
신약 개발 과정에서 약물의 실제 효능을 예측하려면 정제 단백질이 아닌 Live Cell 결합력 측정이 필수적입니다. 이는 세포막의 미세환경과 수용체의 본래 구조(native structure)를 그대로 유지한 상태에서 실제 생리적 조건을 반영하여 SPR 분석이 가진 한계를 극복하고 임상 실패 리스크를 최소화하기 때문입니다.
1. 연구 현장의 고민: “왜 SPR 데이터와 임상 결과가 다를까?”
많은 바이오 연구자들이 후보 물질 스크리닝 단계에서 SPR(Surface Plasmon Resonance)을 활용합니다. 하지만 정교하게 설계된 실험임에도 불구하고, 실제 동물 실험이나 임상 단계에서 예상했던 결합력(Affinity)이 나오지 않아 당황하는 경우가 많습니다.
이러한 현상이 발생하는 이유는 대부분 측정 환경의 차이에 있습니다. 인위적인 칩 표면에 단백질을 고정하는 방식은 세포막의 복잡한 물리적 환경을 반영하지 못하며, 이는 실제 생체 내 약물 효능을 과소/과대 평가하게 만드는 주요 원인이 됩니다.
2. 핵심 용어 정리 (Glossary)
실험 설계 및 데이터 해석의 정확도를 높이기 위해 반드시 숙지해야 할 주요 용어들입니다.
- • Live Cell Assay: 살아있는 세포를 이용하여 약물과 수용체 간의 상호작용을 측정하는 분석법입니다.
- • SPR (Surface Plasmon Resonance): 표면 플라즈몬 공명을 이용해 단백질 간 결합력을 측정하는 전통적 방식이나, 정제된 단백질을 칩에 고정해야 하는 한계가 있습니다.
- • Avidity (다중 결합력): 개별 결합력(Affinity)의 합보다 큰, 세포 표면에서의 전체적인 결합 세기를 의미합니다.
- • Native Structure: 단백질이 생체 내에서 가지는 본래의 3차원 입체 구조입니다.
- • ka (Association rate): 리간드와 수용체가 결합하는 속도 상수를 나타냅니다.
- • kd (Dissociation rate): 결합된 리간드와 수용체가 해리되는 속도 상수입니다.
- • KD (Equilibrium Dissociation Constant): 평형 해리 상수로, 값이 낮을수록 결합력이 강함을 의미합니다. (KD = kd / ka)
3. Live Cell 결합력 측정이 정확한 기술적 근거
살아있는 세포를 기반으로 한 분석(Live Cell Assay)은 단순한 실험법의 차이를 넘어, 생물학적 진실성을 담보하는 기술적 우위를 가집니다. (Reference: ycluebio.com, 2024)
(1) 수용체의 Native 구조 및 모빌리티 유지
단백질을 정제하여 고정하는 과정에서 폴딩(Folding) 변형이 발생할 수 있습니다. 반면, Live Cell 결합력 측정은 세포막에 박혀 있는 수용체의 유동성(Mobility)과 주변 지질막의 영향을 그대로 반영합니다. 이는 실제 약물이 투여되었을 때 맞닥뜨리는 환경과 100% 일치합니다.
(2) Avidity(다중 결합) 효과의 반영
세포 표면에서는 수용체가 클러스터링(Clustering)되어 존재하기도 합니다. 단일 결합력이 약하더라도 여러 곳에서 동시에 결합하는 Avidity 효과가 발생하는데, 이는 오직 살아있는 세포에서만 관찰 가능한 변수입니다.
SPR 데이터에서 KD 값이 지나치게 높게(약하게) 나온다면, 이는 수용체 주변의 Steric hindrance(입체 장애)가 무시되었기 때문일 수 있습니다. 이럴 때는 LigandTracer와 같은 시스템을 통해 실제 세포 표면 결합을 확인하는 검증 단계가 필수적입니다.
4. SPR 분석 vs Live Cell Assay 기술 비교
| 비교 항목 | 전통적 SPR 분석 | Live Cell Assay (LigandTracer) |
|---|---|---|
| 측정 대상 | 정제 단백질 (Purified) | 살아있는 세포 표면 수용체 |
| 측정 환경 | 인위적 금(Gold) 칩 표면 | 실제 세포막 구조 유지 |
| 결합 모델 | 1:1 단순 결합 모델 | Avidity, 이질 결합 모델 포함 |
| 생체 관련성 | 낮음 (폴딩 변형 위험) | 매우 높음 (Native presentation) |
5. 성공적인 세포 기반 결합 분석을 위한 워크플로우
실제 실험에서 신뢰도 높은 데이터를 얻기 위해 LigandTracer 시스템을 활용한 표준 프로토콜을 준수해야 합니다.
- 01 세포 준비 및 안정화: 타겟 수용체(예: HER2, PD-L1)가 발현된 세포를 Petri dish 한쪽에 배양하고 37도 환경에서 최소 1시간 이상 안정화합니다.
- 02 배경 신호(Blank) 스캔: 회전 모드를 통해 세포가 없는 영역의 신호를 10-15분간 측정하여 노이즈를 실시간 보정합니다.
- 03 결합(Association) 및 해리(Dissociation): 리간드를 투입하여 ka를 측정하고(60-120분), 이후 리간드가 없는 배지로 교체하여 kd를 기록합니다(120-240분).
자주 묻는 질문(FAQ)
Q1. 세포 결합 분석 시 비특이적 결합은 어떻게 해결하나요?
A1. LigandTracer 시스템은 디쉬를 회전시키며 실시간으로 빈 공간(blank)을 스캔합니다. 이를 통해 리간드가 용액 중에 존재하며 생기는 노이즈를 자동으로 감쇄하여 신뢰할 수 있는 데이터만 남깁니다.
Q2. 정제 단백질 실험 결과보다 KD 값이 낮게(강하게) 나오는 이유는 무엇인가요?
A2. 주로 세포 표면에서의 Avidity 효과 때문입니다. 실제 생체 내 환경에서는 여러 수용체가 협동적으로 리간드에 결합하므로 단일 단백질 테스트보다 훨씬 강력한 결합력을 보일 수 있습니다.
문의 QR 코드 (메시지 연결)