실시간 결합 분석 기술 선택 시, 정밀한 kinetics 데이터와 소분자 분석이 목적이라면 고감도 SPR을, 세포 용해물과 같은 조잡 샘플의 빠른 스크리닝이 우선이라면 고처리량 BLI를 선택하는 것이 가장 효율적입니다. SPR은 미세유체 채널을 통해 10pM 수준의 고감도를 제공하며, BLI는 ‘Dip and Read’ 방식으로 96/384웰의 대량 샘플을 신속하게 처리할 수 있어 실험 목적에 따른 명확한 기준 설정이 필요합니다.
SPR BLI 분석 실험 선택 기준: 기술 원리와 강점
바이오 의약품 개발 과정에서 SPR(Surface Plasmon Resonance)과 BLI(Bio-Layer Interferometry)는 라벨 프리 실시간 결합 분석의 양대 산맥입니다. 하지만 두 기술은 물리적 감지 원리와 샘플 핸들링 방식에서 뚜렷한 차이를 보입니다.
금속 표면의 굴절률 변화를 미세유체 채널 내에서 감지합니다. 정제된 샘플을 사용하며, 아주 미세한 신호 변화도 잡아낼 수 있어 저분자(Small molecule) 및 고정밀 Kinetics 분석에 필수적입니다.
광섬유 팁 끝의 간섭 패턴 변화를 측정하는 ‘Dip and Read’ 방식입니다. 유로(Fluidics)가 없어 막힘 걱정이 없으므로 세포 용해물이나 혈청 같은 조잡 샘플(Crude sample) 분석에 매우 유리합니다.
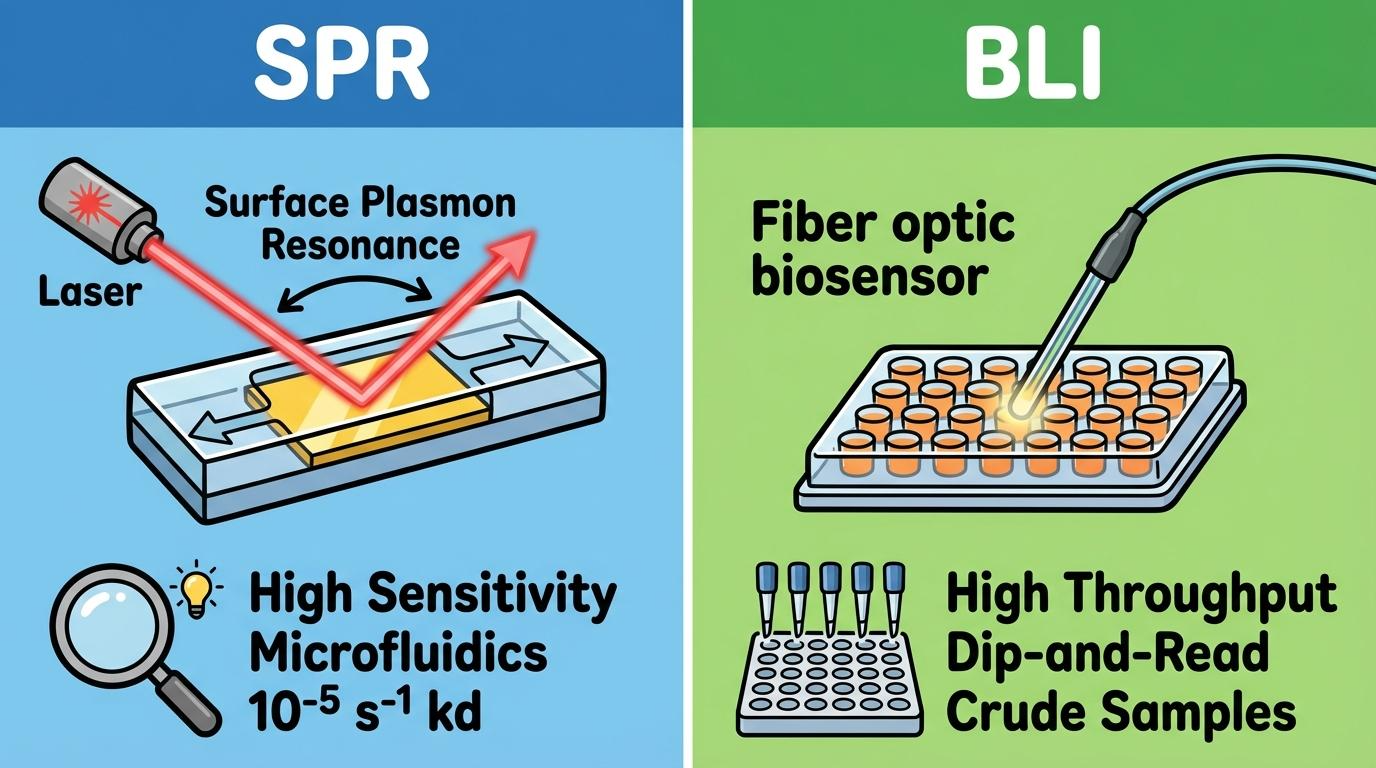
[그림 1] SPR의 미세유체 유로 시스템 vs BLI의 센서 딥핑 방식 구조적 차이
기술 사양 상세 비교
연구 현장에서 가장 체감되는 두 기술의 수치적 성능 차이를 아래 표로 정리했습니다.
| 비교 항목 | SPR (Biacore T200 기준) | BLI (Octet RED96 기준) |
|---|---|---|
| 감도 (해리 속도 kd) | 최대 10-5 s-1 (매우 높음) | 최대 10-4 s-1 (중간) |
| 처리량 (Throughput) | 중저속 (1-8 채널 정밀 분석) | 고속 (96/384 웰 동시 스크리닝) |
| 샘플 유형 | 고도로 정제된 샘플 권장 | 원액, 세포 용해물, 혈청 가능 |
| 최소 분석물 크기 | < 100 Da (소분자 가능) | > 5000 Da (단백질 위주) |
실험 목적별 최적의 선택 가이드
1. 대량 스크리닝인가, 정밀 Kinetics 분석인가?
수백 개의 항체 후보군 중 결합력이 있는 것을 빠르게 골라내야 하는 1차 스크리닝 단계라면 BLI가 압도적으로 유리합니다. 반면, 선별된 후보 물질의 정확한 결합 속도 상수(ka)와 해리 속도 상수(kd)를 측정하여 biophysics 데이터를 논문에 싣거나 IND 승인을 준비한다면 SPR의 정밀한 baseline이 반드시 필요합니다.
2. 샘플의 상태와 정제도
실험실에서 갓 추출한 세포 용해물이나 정제가 어려운 복합 샘플을 다룬다면 BLI를 선택하십시오. SPR은 미세유체 유로가 막힐 위험이 있어 샘플 전처리에 많은 시간이 소요될 수 있습니다.
“BLI로 스크리닝하고, SPR로 검증하라”
초기 벤처 기업이나 신약 개발 팀에서 가장 많이 쓰이는 전략입니다. 조잡 샘플에서 BLI로 유효성을 신속히 확인한 후, 선별된 최종 후보 물질(Lead compound)에 대해서만 정제 과정을 거쳐 SPR로 고정밀 데이터를 산출하면 시간과 비용을 획기적으로 줄일 수 있습니다.
실제 실험 프로토콜 예시
SPR 프로토콜 (정밀 분석)
- 칩 준비: CM5 칩 활성화 (EDC/NHS 혼합물 주입)
- 고정화: 리간드(10-50 µg/mL)를 pH 4.5 버퍼로 고정 (목표 500 RU)
- 샘플 주입: 분석물(1.25-80 nM)을 30-100 µL/min 유속으로 주입
- 분석: Trace Drawer 소프트웨어로 Double-reference subtraction
- 재생: 10 mM Glycine-HCl (pH 2.0)로 표면 세척
BLI 프로토콜 (고속 스크리닝)
- 센서 준비: 전용 센서를 kinetics 버퍼에서 10분간 Hydration
- 로딩: 항원(5-10 µg/mL)에 센서를 300초간 침지(Dip)
- 결합: 항체 샘플이 담긴 96웰 플레이트에 센서를 담가 결합 측정
- 해리: 버퍼 웰로 옮겨 1000초간 해리 과정 관찰
- 자동화: 96개 샘플을 일괄 설정하여 무인 운전 가능
핵심 용어 정리 (Glossary)
- • ka (Association rate constant)
- 두 분자가 결합하는 속도를 나타내는 상수로, 값이 클수록 빠르게 결합함을 의미합니다. 단위는 M-1s-1입니다.
- • kd (Dissociation rate constant)
- 결합된 복합체가 떨어져 나가는 속도로, SPR은 10-5 s-1 수준의 매우 느린 해리(강한 결합)도 정확히 감지할 수 있습니다.
- • KD (Equilibrium Dissociation Constant)
- 평형 상태에서의 해리 상수로, 결합 친화도(Affinity)를 나타내는 가장 중요한 지표입니다 (KD = kd / ka). 값이 작을수록 친화도가 높습니다.
- • Mass-transport limitation
- 분자가 센서 표면으로 이동하는 속도가 결합 속도보다 느려 데이터가 왜곡되는 현상입니다. 고유속 SPR 실험에서 특히 주의해야 합니다.
자주 묻는 질문 (FAQ)
A. SPR이 절대적으로 유리합니다. 소분자는 결합 시 발생하는 신호 변화가 매우 미미하므로, baseline 노이즈가 적고 감도가 높은 SPR 시스템이 훨씬 정확한 데이터를 제공합니다.
A. 전혀 그렇지 않습니다. 다만 BLI는 흔들림(Agitation) 방식을 사용하므로 확산 제한이 발생할 수 있습니다. 이를 보정하기 위해 Stirring 속도를 최적화하고 검증된 프로토콜을 사용한다면 충분히 신뢰도 높은 데이터를 얻을 수 있습니다.
A. BLI가 유리합니다. SPR은 정교한 미세유체 펌프와 밸브 시스템이 있어 주기적인 필터 교체 및 전문 엔지니어의 관리가 필요하지만, BLI는 팁 기반 시스템이라 상대적으로 유지보수가 간편하고 비용이 낮습니다.
내 연구에 딱 맞는 분석 기술을 찾고 계신가요?
실험 설계 및 장비 선정 전문가 문의하기문의 QR 코드 (메시지 연결)