성공적인 리드 항체 선정(Lead Antibody Selection)을 위해서는 단순한 결합력을 넘어 기능성 어세이를 통한 생물학적 활성 검증과 약물성 평가(Developability)를 통한 생산 공정 최적화 가능성을 반드시 확인해야 합니다. 특히 히트(Hit) 단계에서 걸러진 수많은 후보 중 임상 가능성이 높은 물질을 선별하는 것이 비용 손실을 줄이는 핵심입니다.
현장의 고민: 수백 개의 후보군 중 ‘진짜’는 누구인가?
항체 신약 개발 현장에서 연구원들이 가장 고심하는 순간은 스크리닝을 통해 얻은 수많은 히트(Hit) 항체 중, 임상 단계까지 살아남을 ‘리드 항체’를 결정하는 시점일 것입니다. 단순히 “가장 잘 붙는 항체”를 선택했다가 나중에 생산 수율이 나오지 않거나, 비특이적 결합으로 인한 독성 문제로 프로젝트가 중단되는 사례를 빈번하게 목격하곤 합니다.
히트(Hit) 항체: 원석에서 보석으로 가는 첫 단계
리드 선정(Lead Selection)을 이해하기 위해 먼저 히트(Hit) 항체의 개념을 정립해야 합니다. 히트 항체는 라이브러리 스크리닝(Phage Display, Hybridoma 등) 직후 얻어지는 ‘1차 후보군’입니다.
히트(Hit) 항체의 주요 특성
- ✅ 단계: 초기 스크리닝(Screening) 완료 직후
- ✅ 특성: 타겟 항원에 대해 ‘특이적 결합(Specific Binding)’이 확인된 상태
- ✅ 상태: 아직 최적화(Optimization)되지 않은 야생형(Wild-type)에 가까운 서열
- ✅ 규모: 적게는 수십 개에서 많게는 수백, 수천 개의 클론(Clone)
* 즉, 히트 항체는 “타겟에 붙기는 하지만, 약으로서의 성능(효능, 안전성, 생산성)은 아직 검증되지 않은 원석”과 같습니다.
대부분의 연구팀이 범하는 치명적인 오해
많은 경우 후보물질 검증 과정에서 히트 항체의 결합 친화도(Affinity, KD) 수치에만 매몰되곤 합니다. “KD 값이 pM(Pico-molar) 단위니까 무조건 최고의 리드다”라고 판단하는 것이죠. 하지만 실제 임상 성공을 위해서는 항체가 우리 몸 안에서 얼마나 안정적으로 유지되는지, 그리고 세포 내에서 의도한 기능을 정확히 수행하는지가 훨씬 중요합니다.
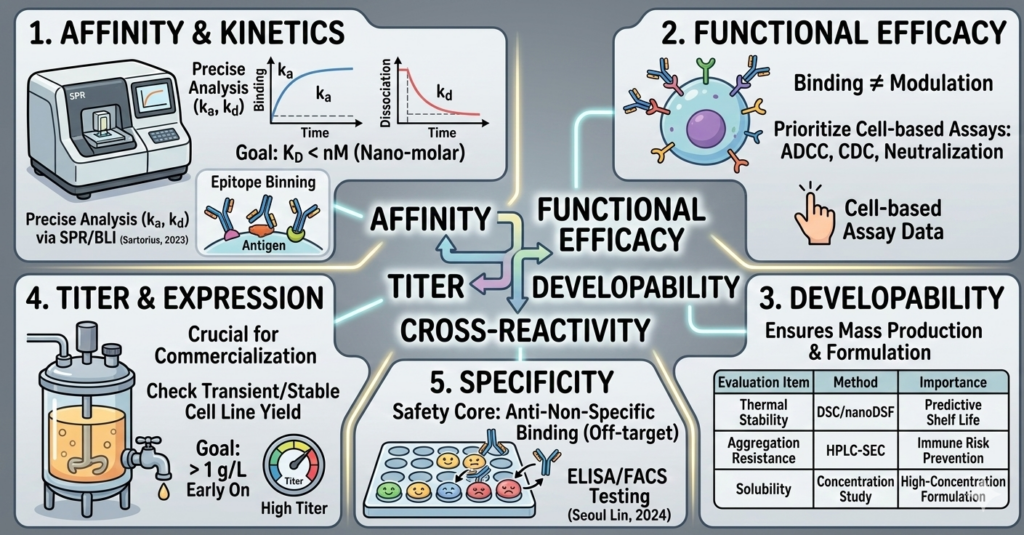
Lead Antibody Selection 시 반드시 체크해야 할 5가지 기준
1. 친화도 및 결합 특성 (Affinity & Kinetics)
단순 ELISA 결과가 아닌, SPR(Surface Plasmon Resonance)이나 BLI(Bio-Layer Interferometry) 장비를 통해 결합 속도(ka)와 해리 속도(kd)를 정밀하게 분석해야 합니다. (Sartorius, 2023)
- 기준 수치: 일반적으로 KD < nM (Nano-molar) 수준의 높은 친화도를 목표로 합니다.
- 에피토프 비닝(Epitope Binning): 타겟 항원의 서로 다른 부위에 결합하는 항체들을 그룹화하여 교차 반응성을 사전에 배제합니다.
2. 기능성 어세이 결과 (Functional Efficacy)
항체가 타겟에 ‘붙는 것’과 타겟을 ‘조절하는 것’은 다른 문제입니다. 기능성 어세이를 통해 실제 생물학적 활성을 확인해야 합니다.
3. 약물성(Developability) 평가
실험실 수준을 넘어 대량 생산과 제형화가 가능한지를 평가하는 단계입니다. 약물성 평가를 간과하면 공정 개발(CMC) 단계에서 막대한 비용이 발생합니다.
| 평가 항목 | 주요 분석법 | 중요성 |
|---|---|---|
| 열안정성 | DSC / nanoDSF | 항체의 구조적 안정성 및 유효기간 예측 |
| 응집 저항성 | HPLC-SEC | Aggregation으로 인한 면역원성 위험 방지 |
| 용해도 | Concentration Study | 고농도 제형 가능 여부 확인 |
4. 생산성 및 발현 수준 (Titer)
아무리 효능이 좋아도 생산 수율이 낮으면 상업화가 불가능합니다. Transient 또는 Stable cell line에서의 발현량을 체크합니다.
목표 수치 예시: 초기 단계에서도 최소 1 g/L 이상의 Titer를 확보할 수 있는 Sequence를 선택하는 것이 유리합니다.
5. 특이성 및 종간 교차반응성 (Specificity & Cross-reactivity)
종간 교차반응성이란 인간(Human) 타겟을 목표로 개발된 항체가 다른 생물종(예: 마우스, 원숭이)의 동일 타겟 단백질에도 유사한 수준으로 결합하는 특성을 의미합니다.
- 전임상 평가의 효율성: 원숭이(NHP) 등 동물 모델과 교차반응이 있다면, 임상 진입 전 독성과 효능을 실제 약물 후보로 직접 테스트할 수 있습니다.
- 안전성 보장: 타겟 종에서의 Off-target binding 여부를 확인하여 인체 내 비특이적 결합으로 인한 부작용을 사전에 예측합니다.
- 비용 및 시간 절감: 교차반응이 없는 경우 대리 항체(Surrogate antibody)를 별도 제작해야 하므로, 개발 기간이 늘어나고 데이터의 일관성이 떨어질 위험이 있습니다.
따라서 리드 항체 선정 시 ELISA나 FACS를 통해 주요 실험 동물 종과의 결합력을 반드시 대조 확인해야 하며, 비특이적 결합이 없는 클론을 선별하는 것이 필수적입니다. (Seoul Lin, 2024)
전문 용어 정리 (Glossary)
- Hit Antibody: 타겟에 대한 결합력은 확인되었으나 기능 및 약물성 검증 전인 초기 항체 클론.
- Epitope Binning: 타겟 항원의 결합 부위(Epitope)에 따라 항체들을 그룹화하는 기술로, 경쟁적 결합 여부를 판단하는 데 쓰입니다.
- Species Cross-reactivity: 인간용 항체가 다른 종(마우스, 원숭이 등)의 동일 타겟에도 결합하는 성질. 전임상 독성 시험의 필수 요건입니다.
- KD (Equilibrium Dissociation Constant): 평형 해리 상수. 값이 낮을수록 친화도가 높음을 의미합니다.
- SPR (Surface Plasmon Resonance): 표면 플라즈몬 공명. 분자 간의 결합 및 해리 과정을 실시간으로 분석하는 기술입니다.
- ADCC (Antibody-Dependent Cellular Cytotoxicity): 항체 의존성 세포 독성. 항체가 타겟 세포에 붙어 면역세포의 공격을 유도하는 기전입니다.
자주 묻는 질문 (FAQ)
Q1. 히트(Hit) 항체 중에서 리드(Lead)를 고를 때 가장 먼저 탈락시켜야 할 조건은?
A1. 비특이적 결합(Non-specific binding)이 나타나는 클론입니다. 결합력이 아무리 좋아도 정상 세포에 붙는다면 독성 문제로 인해 개발이 불가능합니다.
Q2. Developability 평가는 언제 시작하는 것이 가장 좋나요?
A2. 리드 항체를 최종 확정하기 직전인 Lead Optimization 단계에서 병행하는 것이 가장 효율적입니다. 너무 늦어지면 구조적 결함이 발견되었을 때 되돌리기 어렵습니다.
문의 QR 코드 (메시지 연결)