차세대 항체 개발의 성공은 에피토프 비닝 (Epitope Binning)을 통한 후보물질의 효율적 그룹화와 에피토프 매핑 (Epitope Mapping)을 통한 정밀 결합 부위 규명에 달려 있습니다. 이 기술들을 활용하면 수천 개의 후보 중 중복을 제거하고 강력한 지적재산권(IP)을 확보할 수 있으며, 특히 HT-SPR과 HDX-MS 기술을 결합하여 임상 단계에서의 불확실성을 30% 이상 낮출 수 있습니다.
핵심 키워드: #에피토프비닝 #에피토프매핑 #HT-SPR #HDX-MS #항체신약
1. 에피토프 비닝 (Epitope Binning): 수천 개의 항체 중 ‘진짜’를 선별하는 법
항체 라이브러리 스크리닝 단계에서 연구원들이 가장 흔히 겪는 문제는 “결합력(Affinity)은 좋지만, 실제 기능적으로 유효한 위치에 결합하는가?”를 빠르게 판단하지 못하는 것입니다. 단순히 결합 여부만 확인하는 방식은 중복된 에피토프를 가진 항체들을 걸러내지 못해 후기 공정에서 막대한 시간과 비용 손실을 초래합니다. 따라서 정밀한 에피토프 비닝 (Epitope Binning)과 항원 결합 부위 분석이 초기 단계에서 선행되어야 합니다.
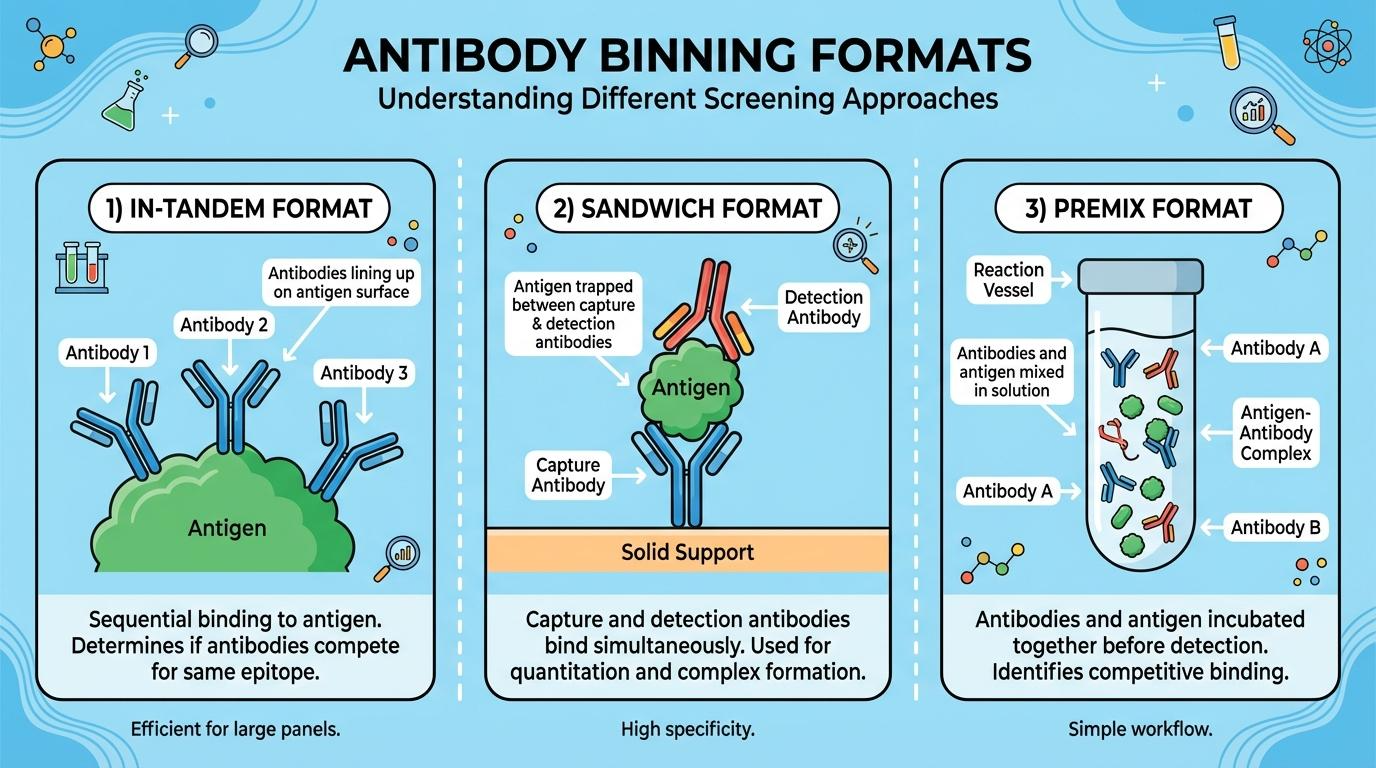
그림 1: 에피토프 비닝(Epitope Binning)의 주요 분석 포맷 비교
최근 연구 데이터에 따르면, 초기 단계에서 비닝을 생략했을 때 발생하는 ‘Redundant Leads(중복 후보)’ 비율은 약 40~60%에 달합니다. 이는 벤처 기업의 한정된 리소스를 낭비하는 주범입니다.
2. 대부분이 오해하는 Binning과 Mapping의 기술적 경계
많은 연구자들이 에피토프 비닝 (Epitope Binning)만으로 결합 아미노산을 알 수 있다고 오해하곤 합니다. 하지만 두 기술은 목적과 해상도 면에서 명확히 구분됩니다.
- Epitope Binning: “이 항체들이 서로 같은 곳에 붙으려고 싸우는가?” (그룹화, 상대적 관계 파악)
- Epitope Mapping: “항원의 몇 번째 아미노산에 정확히 결합하는가?” (좌표 확정, 절대적 위치 규명)
3. 에피토프 비닝 (Epitope Binning)의 3가지 핵심 포맷
에피토프 비닝은 HT-SPR(High-Throughput Surface Plasmon Resonance) 기술을 통해 수행되며, 샘플 소모를 90% 이상 절감하면서 분석 시간을 며칠 단위에서 단 몇 시간으로 단축할 수 있습니다.
| 분석 포맷 | 주요 특징 | 분석 효율성 |
|---|---|---|
| In-Tandem | 항원 고정 후 항체들을 순차적으로 주입하여 경쟁 확인 | 중간 (준비 과정 단순) |
| Sandwich | 첫 번째 항체 포획 후 항원과 두 번째 항체 주입 | 높음 (고정밀 상호작용 분석) |
| Premix | 항원과 항체를 미리 혼합하여 평형 도달 후 주입 | 매우 높음 (평형 상태 경쟁력 확인) |
HT-SPR 결과에서 Bin 수가 5개 이상 확보된다면 라이브러리의 다양성이 우수한 것으로 판단합니다. 예를 들어 384-well 플레이트 하나로 하루 만에 100개 이상의 항체 쌍을 분석할 수 있어, 기존 ELISA 방식 대비 비용을 약 70% 절감할 수 있습니다.
4. 정밀 Epitope Mapping: 선형 vs 구조적 에피토프
항체-항원 결합의 90% 이상은 구조적 에피토프(Conformational Epitope)입니다. 이는 단백질의 3차원적 접힘 상태에서만 형성되므로, 단순히 아미노산 서열만 보는 펩타이드 스캐닝으로는 한계가 있습니다.
HDX-MS를 활용한 정밀 분석
구조적 에피토프를 정밀 분석하기 위해서는 HDX-MS(수소-중수소 교환 질량분석법)가 필수적입니다. 이 기술은 항원-항체 결합 시 용매에 노출되는 부위의 중수소 교환 속도 변화를 측정하여 실제 3차원 공간에서의 결합 부위를 규명합니다. 이를 통해 아미노산 하나하나의 기여도를 정량화할 수 있습니다.
5. 항체 에피토프 분석 결과 해석 및 IP 전략
항체 에피토프 분석 결과는 보통 Heatmap(열지도)과 Network Cluster로 시각화됩니다. 서로 다른 Bin에 속하는 항체들은 공간적으로 중첩되지 않는 에피토프를 의미하며, 이는 조합 치료제(Combination Therapy) 개발의 핵심 근거가 됩니다.
에피토프 매핑 데이터는 특허 청구 범위에서 ‘구조적 결합 부위’를 명시하는 데 사용됩니다. 아미노산 서열뿐만 아니라 ‘A 위치에서 B 위치까지의 입체적 결합’을 입증함으로써 타사의 특허 회피를 효과적으로 방어할 수 있습니다.
📚 핵심 용어 정리 (Glossary)
• HT-SPR: High-Throughput Surface Plasmon Resonance. 대량의 시료를 고속으로 분석하여 결합 속도(ka)와 해리 속도(kd)를 실시간 측정하는 기술.
• HDX-MS: Hydrogen-Deuterium Exchange Mass Spectrometry. 단백질 구조의 동역학과 상호작용 부위를 질량 차이로 분석하는 고정밀 기법.
• Redundant Leads: 결합 부위가 동일하여 기능적으로 중복되는 항체 후보군.
• SCM (Surface Concentration Mapping): 항체 고정 밀도를 조절하여 최적의 분석 조건을 찾는 전처리 단계.
자주 묻는 질문 (FAQ)
일반적으로 20~30개 이상의 라이브러리가 확보되었을 때 비닝의 통계적 유의미함이 나타납니다. 하지만 10개 내외의 소수 후보군이라도 IP 확보를 위해 비닝을 수행하는 것이 권장됩니다.
네, 가능합니다. 비닝은 ‘입체적 장애(Steric Hindrance)’를 포함한 상대적 경쟁을 보지만, 매핑은 실제 ‘물리적 결합 잔기’를 찾기 때문입니다. 따라서 두 데이터를 상호 보완적으로 해석하는 전문가의 안목이 중요합니다.
- Bioresearch Today (2024), “Advancements in High-Throughput Epitope Binning for Antibody Discovery.”
- Journal of Protein Science, “Hydrogen-Deuterium Exchange Mass Spectrometry in Conformational Mapping.”
- FDA Guidance for Industry, “Analytical Procedures and Methods Validation for Drugs and Biologics.”
* 본 포스팅에 언급된 특정 기술명은 해당 상표권자의 자산이며, 정보 제공 목적으로만 사용되었습니다.
문의 QR 코드 (메시지 연결)